
分析 设该烃的分子式为CnH2n+2,烃和氯气发生取代反应生成氯代烃和HCl,反应方程式为CnH2n+2+Cl2$\stackrel{光照}{→}$CnH2n+1Cl+HCl,放出的气体恰好被500mL0.2mol/L的氢氧化钠溶液中和,发生反应HCl+NaOH=NaCl+H2O,该反应中n(HCl)=n(NaOH)=0.2mol/L×0.5L=0.1mol,根据取代反应方程式知,n(HCl)=n(CnH2n+2)=0.1mol,根据M=$\frac{m}{n}$计算其摩尔质量,从而计算n值,再根据其一氯取代物种类确定结构简式.
解答 解:设该烃的分子式为CnH2n+2,烃和氯气发生取代反应生成氯代烃和HCl,反应方程式为CnH2n+2+Cl2$\stackrel{光照}{→}$CnH2n+1Cl+HCl,放出的气体恰好被500mL0.2mol/L的氢氧化钠溶液中和,发生反应HCl+NaOH=NaCl+H2O,该反应中n(HCl)=n(NaOH)=0.2mol/L×0.5L=0.1mol,根据取代反应方程式知,n(HCl)=n(CnH2n+2)=0.1mol,烃的摩尔质量M=$\frac{m}{n}$=$\frac{7.2g}{0.1mol}$=72g/mol,物质的摩尔质量在数值上等于其相对分子质量,则12n+2n+2=72,n=5,所以该烃是戊烷,该烃的一氯取代物有一种,则该烃为2,2-二甲基丙烷,其结构简式为C(CH3)4,
答:该烃的分子式为C5H12,结构简式为C(CH3)4.
点评 本题考查了有机物分子式及结构简式的确定,明确取代反应时各个物理量之间的关系是解本题关键,再结合物质的量、摩尔质量、质量、相对分子质量之间的关系式解答,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Cu与浓硝酸反应制备NO2:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O | |
| B. | NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-═AlO2-+2H2O | |
| C. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| D. | 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 误将洁厕灵与84消毒液混合:H++Cl-+HClO=Cl2↑+H2O | |
| C. | 酸性高锰酸钾和过氧化氢制取少量氧气:2MnO4-+12H++4H2O2═4Mn2++7O2↑+10H2O | |
| D. | 用0.3mol/L的氯化铵溶液除去氢氧化铝中少量的氢氧化镁:Mg(OH)2+2NH4+=Mg2++2NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 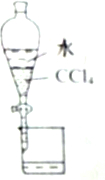 分离CCl4和水 | |
| B. |  洗涤沉淀时,向漏斗中加适量水,搅拌并滤干 | |
| C. |  液体分层,下层呈无色 | |
| D. |  除去氯气中的氯化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol•L-1) | 0.8 | 1.24 | 1.24 |
| A. | 平衡后升高温度,平衡常数>400 | |
| B. | 平衡时,c(CH3OCH3)=1.6 mol•L-1 | |
| C. | 平衡时,反应混合物的总能量减少40 kJ | |
| D. | 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
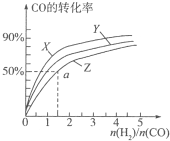 甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 除⑤外 | C. | 除①外 | D. | 除①、⑤外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).
;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com