
 的系统命名法的名称3,3,5,-三甲基庚烷
的系统命名法的名称3,3,5,-三甲基庚烷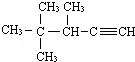 的系统命名法的名称为3,4,4-三甲基-1-戊炔.
的系统命名法的名称为3,4,4-三甲基-1-戊炔. .
. 分析 (1)2-甲基-3-乙基戊烷,主碳链5个碳,2号碳有一个甲基,3号碳有一个乙基;
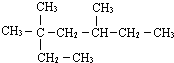
(2)选取最长碳链含7个碳,离取代基近的一端编号,据此书写名称;
(3)物质为炔烃,选取含碳碳三键的最长碳链为主碳链,离三键近的一端编号得到名称;
(4)首先写出结构式,根据结构式再写出键线式;碳碳键用线段来表现,画出键线式.拐点和端点表示碳原子,碳原子,H不必标出,杂原子(非碳、氢原子)不得省略,并且其上连有的氢也一般不省略.
解答 解:(1)2-甲基-3-乙基戊烷,主碳链5个碳,2号碳有一个甲基,3号碳有一个乙基,得到结构简式为:CH3CH(CH3)-CH(CH2CH3)-CH2CH3,
故答案为:CH3CH(CH3)-CH(CH2CH3)-CH2CH3:
(2)选取最长碳链含7个碳,离取代基近的一端编号,取代基位次和最小,得到物质的名称为:3,3,5,-三甲基庚烷,故答案为:3,3,5,-三甲基庚烷;
(3)物质为炔烃,选取含碳碳三键的最长碳链为主碳链,离三键近的一端编号得到名称,命名为:3,4,4-三甲基-1-戊炔,故答案为:3,4,4-三甲基-1-戊炔;
(4)2-甲基-1,3-丁二烯的结构简式为 所以键线式为
所以键线式为 ,
,
故答案为: ;
;
点评 本题主要考查了有机物结构简式的书写、命名及甲烷的取代反应,注意掌握常见化学用语的表示方法,掌握有机物的命名原则.要注意掌握有机物的结构特点是解题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KNO3是还原剂,其中N元素被氧化 | |
| B. | 生成物中的N2是氧化产物,K2O是还原产物 | |
| C. | 当氧化产物比还原产物多2.8g时,转移电子$\frac{1}{14}$ mol | |
| D. | 氧化剂与还原剂的物质的量之比5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 W、X、Y、Z 是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10,X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.
W、X、Y、Z 是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10,X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 将稀硫酸和Na2S反应生成的气体通入AgNO3与AgCl组成的浊液中 | Ksp(AgCl)>Ksp(Ag2S) |
| B | 室温下,向浓度均为0.1 mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(BaSO4)<Ksp(CaSO4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe3+的氧化性比I2的强 |
| D | 室温下,用pH试纸测得0.1mol•L-1 Na2SO3溶液的pH约为10;0.1mol•L-1 NaHSO3溶液的pH约为5. | HSO3-结合H+的能力比SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com