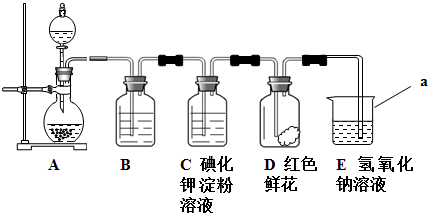
分析:(1)Mg元素原子的3s能级容纳2个电子,为全满稳定状态,能量降低,同周期元素从左到右金属性逐渐减弱;
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
=1,为AlNi,每个Ni原子周围有8个Al原子,每个Al原子周围有8个Ni原子,据此结合选项中各物质的晶胞结构判断;
(3)苯环中存在大π键,碳原子杂化数为2,采取sp
2杂化,侧链中C、O、N原子根据成的单键数目与孤对电子确定杂化轨道数目判断杂化方式;
(4)①根据核外电子排布规律书写;
②Ni
2+含有空轨道,N原子含有孤对电子对,N原子与Ni
2+形成配位键,氧原子与氢原子之间形成氢键.
解答:
解:(1)Mg元素原子的3s能级容纳2个电子,为全满稳定状态,能量降低,第一电离能高于同周期相邻的元素,故第一电离能Al<Mg,
同周期元素从左到右金属性逐渐减弱,因此金属性Al<Mg,
故答案为:<;<;
(2)由图可知铝镍合金的晶胞结构中,Ni原子数目为1,Al原子数目为8×
=1,为AlNi,每个Ni原子周围有8个Al原子,每个Al原子周围有8个Ni原子,
A.氯化钠中每个钠离子周围有6个氯离子,每个氯离子周围有6个钠离子,不符合;
B.氯化铯中每个铯离子周围有8个氯离子,每个氯离子周围有8个铯离子,符合;
C.石英为空间立体网状结构,硅原子周围有4个氧原子,氧原子周围有2个硅原子,不符合;
D.金刚石为空间立体网状结构,每C原子周围有4个C原子,不符合;
故答案为:B;
(3)苯环中存在大π键,碳原子杂化数为2,采取sp
2杂化,侧链中C原子成4个单键,杂化轨道数为4,采取sp
3杂化,O原子成2个单键,含有2对孤对电子,杂化轨道数为4,采取sp
3杂化,N原子成3个单键,含有1对孤对电子,杂化轨道数为4,采取sp
3杂化,
故答案为:C、N、O;
(4)①Ni是28号元素,核外有28个电子,其原子核外电子排布为1s
22s
22p
63s
23p
63d
84s
2,
故答案为:1s
22s
22p
63s
23p
63d
84s
2;
②Ni
2+含有空轨道,N原子含有孤对电子对,N原子与Ni
2+形成配位键,不同分子中氧原子与氢原子之间形成氢键,如图所示:
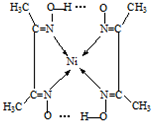
,
故答案为:

.

 ,与其结构相似的化合物是
,与其结构相似的化合物是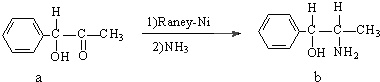
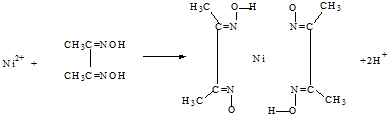
 ,
, .
.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案