
| A. | 锂(Li)与水反应比钠与水反应剧烈 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | HBr的稳定性比HI强 |
分析 A.Na、Li同主族,金属性越强,与水反应越剧烈;
B.卤素单质的颜色随原子叙述的增大而加深,AgCl、AgBr、AgI等均不溶于水和硝酸;
C.碱金属越活泼,与氧气反应生成物越复杂;
D.非金属性越强,气态氢化物越稳定.
解答 解:A.Na、Li同主族,Na的金属性强,则钠与水反应剧烈,故A错误;
B.由卤素单质及AgX的性质的相似性和递变性可知,砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸,故B正确;
C.碱金属越活泼,与氧气反应生成物越复杂,金属性Rb>Na,Na的氧化产物有2种,可知铷(Rb)的燃烧产物比钠的燃烧产物更复杂,故C正确;
D.非金属性Br>I,可知HBr的稳定性比HI强,故D正确;
故选A.
点评 本题考查元素周期表和元素周期律的综合应用,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
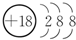 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
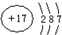 ,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024
,含1mol X 的氧化物晶体中含有共价键数目为4NA或2.408×1024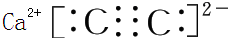
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
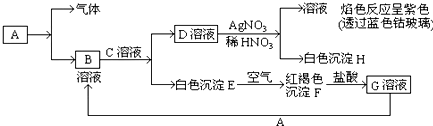
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型.如图,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了分子的球棍模型.如图,下列说法中不正确的是( )| A. | 该烃X与等质量的甲烷相比,X燃烧时消耗的氧气更多 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 分子中的氢原子分布在两个相互垂直的直线上 | |
| D. | 分子中有C-C键,也有C=C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M的能量比G高 | |
| B. | N的能量比G高 | |
| C. | 这一反应不需要加热一定能发生 | |
| D. | 反应物的能量之和大于生成物的能量之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
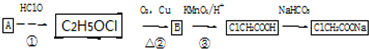
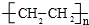 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com