
2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR',反应式可表示为:2RCH=CHR'—→ RCH=CHR + R'CH=CHR'
现有结构简式为CH2=CHCH3和CH2=C(CH3)2的两种烯烃,发生上述的“烯烃复分解反应”,能生成多种新的烯烃。下列说法正确的是
A.生成的新烯烃共有4种
B.生成的各种新烯烃中,每个烯烃分子与HCl加成后,都只能生成一种产物
C.生成的所有新烯烃分子中,每个分子中的碳原子均共面
D.生成的所有新烯烃分子中,只有两种新烯烃分子中的碳原子共面
科目:高中化学 来源: 题型:
| ||
| 500℃ |



| 500℃ |
| 500℃ |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 CH2=CH2+R1CH=CHR2
CH2=CH2+R1CH=CHR2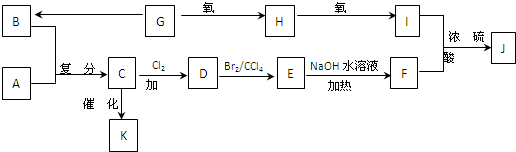




查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
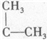 发生“烯烃复分解反应”,生成新烯烃种类为( )
发生“烯烃复分解反应”,生成新烯烃种类为( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com