
【题目】25℃时,下列说法正确的是
A.某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=a+1
B.在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液pH<7
C.NH4Cl溶液的Kw大于NaCl溶液的Kw
D.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中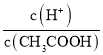 增大
增大
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】实验室模拟工业生产食品香精菠萝酯(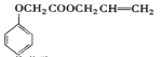 )的简易流程如下:
)的简易流程如下:
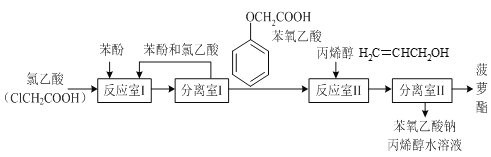
有关物质的熔、沸点如表:
苯酚 | 氯乙酸 | 苯氧乙酸 | |
熔点/℃ | 43 | 62 | 99 |
沸点/℃ | 181.9 | 189 | 285 |
试回答下列问题:
(1)反应室I中反应的最佳温度是104℃,为较好地控制温度在102℃~106℃之间,加热时可选用___(选填字母)。
A.火炉直接加热 B.水浴加热 C.油浴加热
(2)分离室I采取的操作名称是___。
(3)反应室I中发生反应的化学方程式是___。
(4)分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是___(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:X2(g)+3Y2(g) ![]() 2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
2Z2(g),若X2、Y2、Z2的初始物质的量浓度分别为0.10mol·L-1、0.30mol·L-1、0.20mol·L-1,当反应达到平衡时Z2的物质的量浓度不可能是
A. 0.05mol·L-1 B. 0.20mol·L-1 C. 0.35mol·L-1 D. 0.40mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.向0.1molL-1的CH3COOH溶液中加入少量碳酸钙固体,溶液的pH增大
B.室温下,pH=4的NaHSO4溶液中,水电离出的H+浓度为1×10-10molL-1
C.浓度均为0.1molL-1的HCN溶液和NaCN溶液等体积混合(忽略体积变化),溶液中c(HCN)+c(CN-)=0.1molL-1
D.pH相同的①NH4Cl、②NH4Al(SO4)2、③(NH4)2SO4三种溶液的c(NH4+):②<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上用ClO2气体制NaClO2的工艺流程如图所示。
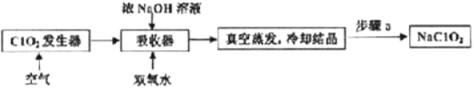
下列说法不正确的是
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO2的离子方程式为2ClO2+H2O2=2ClO2-+2H+ +O2↑
C.工业上将ClO2气体制成NaCIO2固体,其主要目的是便于贮存和运输
D.通入的空气的目的是驱赶出ClO2,使其被吸收其充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某反应A(g)+B(g)=C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题。
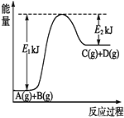
(1)该反应是_____(填“吸热”或“放热”)反应,该反应的ΔH=________kJ/mol (用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量______(填“一定高”“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使反应速率增大,则E1和E2的变化是:E1_______,E2________ΔH______ (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气常用作致冷剂及制取铵盐和氮肥,是一种用途广泛的化工原料.
(1)下表是当反应器中按![]() :
:![]() :3投料后,在
:3投料后,在![]() 、
、![]() 、
、![]() 下,反应达到平衡时,混合物中
下,反应达到平衡时,混合物中![]() 的物质的量分数随压强的变化曲线.
的物质的量分数随压强的变化曲线.
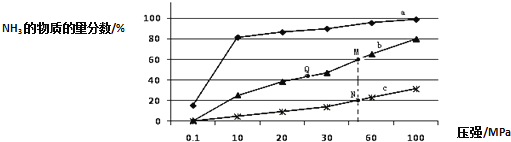
![]() 曲线a对应的温度是 ______ .
曲线a对应的温度是 ______ .
![]() 关于工业合成氨的反应,下列叙述正确的是 ______
关于工业合成氨的反应,下列叙述正确的是 ______ ![]() 填字母
填字母![]() .
.
A.及时分离出![]() 可以提高
可以提高![]() 的平衡转化率
的平衡转化率
B.加催化剂能加快反应速率且提高![]() 的平衡转化率
的平衡转化率
C.上图中M、N、Q点平衡常数K的大小关系是![]()
![]() 点对应的
点对应的![]() 转化率是 ______ .
转化率是 ______ .
(2)工业制硫酸的尾气中含较多的![]() ,为防止污染空气,回收利用
,为防止污染空气,回收利用![]() ,工业上常用氨水吸收法处理尾气.
,工业上常用氨水吸收法处理尾气.
![]() 当氨水中所含氨的物质的量为3mol,吸收标准状况下
当氨水中所含氨的物质的量为3mol,吸收标准状况下![]()
![]() 时,溶液中的溶质为 ______ .
时,溶液中的溶质为 ______ .
![]() 溶液显酸性.用氨水吸收
溶液显酸性.用氨水吸收![]() ,吸收液显中性时,溶液中离子浓度关系正确的是 ______
,吸收液显中性时,溶液中离子浓度关系正确的是 ______ ![]() 填字母
填字母![]() .
.
![]()
![]()
![]()
(3)氨气是一种富氢燃料,可以直接用于燃料电池,下图是供氨水式燃料电池工作原理:
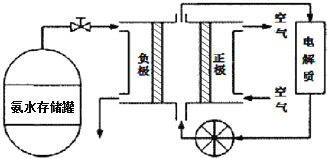
![]() 氨气燃料电池的电解质溶液最好选择 ______
氨气燃料电池的电解质溶液最好选择 ______ ![]() 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性”![]() 溶液.
溶液.
![]() 空气在进入电池装置前需要通过过滤器除去的气体是 ______ .
空气在进入电池装置前需要通过过滤器除去的气体是 ______ .
![]() 氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池正极的电极反应方是 ______ .
氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池正极的电极反应方是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家对CO2的应用研究日新月异。
(1)科学家研制成功一种新型催化剂,能将CO2转变为甲烷。在常压、300℃,CO2与H2体积比为1︰4时在体积为V L的容器中反应,CO2转化率达90%。由图1可知升高温度,K将___(填“增大”“减小”或“不变”);300℃时,从反应开始,到达到平衡,以H2的浓度变化表示化学反应速率是____(用nA、tA、V表示)。
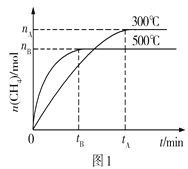
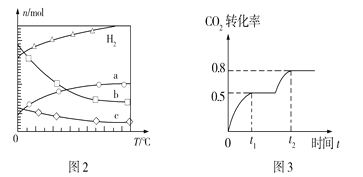
(2)CO2经催化加氢还可合成低碳烯烃有机物:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH=Q kJ·mol1。在0.1MPa时,按n(CO2)︰n(H2)=1︰3投料,图2表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
C2H4(g)+4H2O(g) ΔH=Q kJ·mol1。在0.1MPa时,按n(CO2)︰n(H2)=1︰3投料,图2表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
①Q___0(填“>”“=”或“<”);
②曲线c表示的物质为____;
③为提高CO2的平衡转化率,除改变温度外,还可采取的措施是___。
(3)已知CO2(g)+2CH3OH(g)![]() CH3OCOOCH3(g)+H2O(g)。在恒温容积可变的容器中加入1mol CO2、2mol CH3OH,CO2的转化率与反应时间如图3所示,在反应过程中加压,若t1时容器体积为1000mL,则t2时容器体积为_____mL。
CH3OCOOCH3(g)+H2O(g)。在恒温容积可变的容器中加入1mol CO2、2mol CH3OH,CO2的转化率与反应时间如图3所示,在反应过程中加压,若t1时容器体积为1000mL,则t2时容器体积为_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.常温下,![]() 的氢氧化钠溶液中加入10mL
的氢氧化钠溶液中加入10mL ![]() 的HA,所得溶液
的HA,所得溶液![]()
B.![]() 时,
时,![]() 与
与![]() 的氯化铵溶液的pH前者大
的氯化铵溶液的pH前者大
C.室温时浓度均为![]() 的
的![]() 和
和![]() 的混合液,pH为10,则
的混合液,pH为10,则![]()
D.![]() 溶液:
溶液:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com