
| A£® | Ōö¼ÓĢśµÄĮæ | B£® | ÓĆÅØĮņĖį“śĢęĻ”ĮņĖį | ||
| C£® | ¼ÓČČ | D£® | Ōö“óŃ¹Ēæ |
·ÖĪö Ōö“óĢśĘ¬ÓėĻ”ĮņĖįµÄ·“Ó¦ĖŁĀŹ£¬æÉ“ÓÓ°Ļģ·“Ó¦ĖŁĀŹµÄĶā½ēŅņĖŲĖ¼æ¼£¬æÉŌö“óÅØ¶Č”¢ÉżøßĪĀ¶Č”¢Ōö“ó¹ĢĢåµÄ±ķĆ껿ŅŌ¼°ŠĪ³ÉŌµē³Ų·“Ó¦µČ£®
½ā“š ½ā£ŗA£®Ōö¼ÓĢśµÄÓĆĮ棬¹ĢĢåµÄÅØ¶Č²»±ä£¬·“Ó¦ĖŁĀŹ²»±ä£¬¹ŹA“ķĪó£»
B£®ČēĪŖÅØĮņĖį£¬ŌŚ³£ĪĀĻĀ·¢Éś¶Ū»Æ·“Ó¦£¬²»ÄÜÉś³ÉĒāĘų£¬¹ŹB“ķĪó£»
C£®¼ÓČČ£¬ĪĀ¶ČÉżøߣ¬·“Ó¦ĖŁĀŹŌö“󣬹ŹCÕżČ·£»
D£®·“Ó¦ŌŚČÜŅŗÖŠ½ųŠŠ£¬Ōö“óŃ¹Ē棬·“Ó¦ĖŁĀŹ»ł±¾²»±ä£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģā½Ļ¼ņµ„£¬æ¼²éÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄ³£¼ūŅņĖŲ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ»ł“”ÖŖŹ¶µÄ×ŪŗĻĄķ½āŗĶŌĖÓƵÄæ¼²é£¬Ń§ÉśÓ¦ŹģĻ¤ĪĀ¶Č”¢ÅØ¶Č”¢¹¹³ÉŌµē³Ų”¢Ōö“ó½Ó“„ĆęµČ¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģĄ“½ā“š£¬µ«ÅØĮņĖįµÄŠŌÖŹŹĒѧɜ½ā“šÖŠČŻŅ×ŗöĀŌµÄÖŖŹ¶£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŪµć½Ļøߣ¬Ó²¶Č½Ļ“ó | B£® | Ņ×ČÜÓŚĖ®¶ųÄŃČÜÓŚÓŠ»śČܼĮ | ||
| C£® | ¹ĢĢåŹ±²»Äܵ¼µē | D£® | Ąė×Ó¼ä¾ąĄė½Ļ“ó£¬ĘäĆÜ¶Č½ĻŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
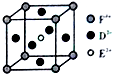 A”¢B”¢C”¢D”¢E”¢FŹĒĒ°ĖÄÖÜĘŚŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĮłÖÖŌŖĖŲ£®AŌŖĖŲŌ×ÓµÄŗĖĶāµē×ÓŹżµČÓŚĘäµē×Ó²ćŹż£¬BŌŖĖŲ»łĢ¬Ō×ÓÓŠČżøöÄܼ¶ĒŅø÷Äܼ¶µē×ÓŹżĻąĶ¬£¬AÓėDæÉŠĪ³ÉĮ½ÖÖ³£¼ūŅŗĢ¬»ÆŗĻĪļG”¢H£¬ĘäŌ×ÓŹżÖ®±Č·Ö±šĪŖ1£ŗ1ŗĶ2£ŗ1£¬EŌŖĖŲŌ×ÓµÄK”¢L²ćµē×ÓŹżÖ®ŗĶµČÓŚĘäM”¢N²ćµē×ÓŹżÖ®ŗĶ£¬F±»³ĘĪŖ¼ĢĢś”¢ĀĮÖ®ŗóµÄµŚČż½šŹō£¬æÉÓĆÓŚÖĘŌģ·É»ś”¢»š¼ż”¢ČĖŌģĪĄŠĒ”¢ÓīÖę·É“¬µČĮģÓņ£®Ēė»Ų“šĻĀĮŠø÷Ģā£ØÉę¼°ŌŖĖŲĒėÓĆĻąÓ¦»Æѧ·ūŗűķŹ¾£©£ŗ
A”¢B”¢C”¢D”¢E”¢FŹĒĒ°ĖÄÖÜĘŚŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĮłÖÖŌŖĖŲ£®AŌŖĖŲŌ×ÓµÄŗĖĶāµē×ÓŹżµČÓŚĘäµē×Ó²ćŹż£¬BŌŖĖŲ»łĢ¬Ō×ÓÓŠČżøöÄܼ¶ĒŅø÷Äܼ¶µē×ÓŹżĻąĶ¬£¬AÓėDæÉŠĪ³ÉĮ½ÖÖ³£¼ūŅŗĢ¬»ÆŗĻĪļG”¢H£¬ĘäŌ×ÓŹżÖ®±Č·Ö±šĪŖ1£ŗ1ŗĶ2£ŗ1£¬EŌŖĖŲŌ×ÓµÄK”¢L²ćµē×ÓŹżÖ®ŗĶµČÓŚĘäM”¢N²ćµē×ÓŹżÖ®ŗĶ£¬F±»³ĘĪŖ¼ĢĢś”¢ĀĮÖ®ŗóµÄµŚČż½šŹō£¬æÉÓĆÓŚÖĘŌģ·É»ś”¢»š¼ż”¢ČĖŌģĪĄŠĒ”¢ÓīÖę·É“¬µČĮģÓņ£®Ēė»Ų“šĻĀĮŠø÷Ģā£ØÉę¼°ŌŖĖŲĒėÓĆĻąÓ¦»Æѧ·ūŗűķŹ¾£©£ŗ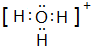 £®
£® ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £®ĻĀĮŠ¹ŲÓŚ±½×ōæØŅņµÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©
£®ĻĀĮŠ¹ŲÓŚ±½×ōæØŅņµÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | ·Ö×ÓŹ½ĪŖC9H10NO2 | |
| B£® | ±½»·ÉĻÓŠ2øöČ”“ś»ł£¬ĒŅŗ¬ÓŠĻõ»łµÄĶ¬·ÖŅģ¹¹ĢåÓŠ6ÖÖ | |
| C£® | 1 moløĆ»ÆŗĻĪļ×ī¶ąÓė4 molĒāĘų·¢Éś¼Ó³É·“Ó¦ | |
| D£® | ·Ö×ÓÖŠŗ¬ÓŠ3ÖÖ¹ŁÄÜĶÅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓƶčŠŌµē¼«µē½āCuSO4ČÜŅŗŗó£¬Čē¹ū¼ÓČė0.1mol Cu£ØOH£©2ÄÜŹ¹ČÜŅŗø“Ō£¬ŌņµēĀ·ÖŠ×ŖŅʵē×ӵďżÄæĪŖ0.2NA | |
| B£® | 28æĖÓÉC3H6ŗĶC4H8×é³ÉµÄ»ģŗĻĘųĢåÖŠŗ¬¹²ÓƵē×Ó¶ŌŹżÄæĪŖ6NAøö | |
| C£® | 0.1molŃõĘų×÷ĪŖŃõ»Æ¼ĮµĆµ½µē×ӵďżÄæŅ»¶ØĪŖ0.4NA | |
| D£® | ³£ĪĀĻĀ£¬0.1mol•L-1µÄĢ¼ĖįÄĘČÜŅŗÖŠŗ¬ÓŠµÄŅõĄė×ÓŹż“óÓŚ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĻÖÓŠĪåÖÖŌŖĖŲ£¬ĘäÖŠA”¢B”¢C”¢D”¢EĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅŌ×ÓŠņŹż¶¼²»³¬¹ż36£®Ēėøł¾ŻĻĀĮŠĻą¹ŲŠÅĻ¢£¬»Ų“šĪŹĢā£®
ĻÖÓŠĪåÖÖŌŖĖŲ£¬ĘäÖŠA”¢B”¢C”¢D”¢EĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅŌ×ÓŠņŹż¶¼²»³¬¹ż36£®Ēėøł¾ŻĻĀĮŠĻą¹ŲŠÅĻ¢£¬»Ų“šĪŹĢā£®| A | »łĢ¬Ō×Ó×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµÄČż±¶ |
| B | »łĢ¬Ō×ÓŗĖĶāÓŠ13ÖÖ²»Ķ¬ŌĖ¶ÆדĢ¬µÄµē×Ó |
| C | ÓėBĶ¬Ņ»ÖÜĘŚ£¬Ō×ÓÖŠĪ“³É¶Ōµē×ÓŹżŹĒĶ¬ÖÜĘŚÖŠ×ī¶ąµÄ |
| D | D2-µÄŗĖĶāµē×ÓÅŲ¼Óėė²Ō×ÓĻąĶ¬ |
| E | ŹĒdsĒųŌ×ÓŠņŹż×īŠ”µÄŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠæĮ£ÓėĻ” HNO3·“Ó¦Öʱø H2 | B£® | ¼ÓČČ·Ö½ā NH4Cl ¹ĢĢåÖĘ NH3 | ||
| C£® | “óĄķŹÆÓėĻ” H2SO4·“Ó¦Öʱø CO2 | D£® | ŃĒĮņĖįÄĘÓėÅØ H2SO4·“Ó¦Öʱø SO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
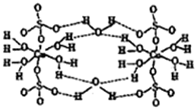 ŅŃÖŖĶŌŖĖŲÄÜŠĪ³É¶ąÖÖ»ÆŗĻĪļ£®
ŅŃÖŖĶŌŖĖŲÄÜŠĪ³É¶ąÖÖ»ÆŗĻĪļ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com