
| A.Fe -2e-= Fe2+ | B.Fe -3e- = Fe3+ |
| C.O2 +2H2O +4e- = 4OH- | D.2H+ + 2e- = H2 ↑ |
科目:高中化学 来源:不详 题型:单选题
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | B.2Fe+2H2O+O2=2Fe(OH)2 |
| C.2H2O+O2+4e- =4OH- | D.Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
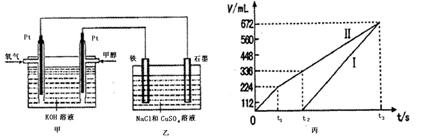
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属腐蚀过程中发生了化学反应 |
| B.在铁表面镀锌可对铁起保护作用 |
| C.在铁船壳上镶嵌铜块能减缓船体的腐蚀 |
| D.铝制品在空气中不易被腐蚀,是因其表面形成了致密的氧化铝保护层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
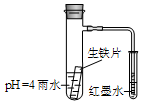
| A.生铁片中的碳是原电池的阳极,发生还原反应 |
| B.雨水酸性较强,生铁片仅发生析氢腐蚀 |
| C.墨水回升时,碳极反应式为:O2 + 2H2O + 4e—= 4OH— |
| D.具支试管中溶液pH逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属腐蚀就是金属失去电子被还原的过程 |
| B.铝制品的耐腐蚀性强,说明铝的化学性质不活泼 |
| C.将海水中钢铁闸门与电源的负极相连,可防止闸门被腐蚀 |
| D.钢铁锈蚀时,铁原子失去电子成为Fe3+,而后生成Fe(OH)3,再部分脱水成为氧化铁的水合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
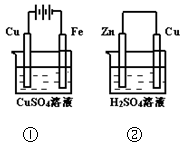
| A.在①中Cu棒为阳极;在②中Cu棒为负极 |
| B.电极上生成物质的质量:①<② |
| C.电极反应式:①中阳极:4OH一一4e一= 2H2O+O2↑;②中负极:2H+ + 2e一= H2↑ |
| D.溶液的pH:①不变;②增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
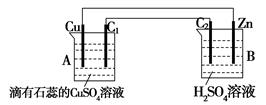
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com