
二甲醚(CH3OCH3)和甲醇(CH3OH)都是高效清洁能源。工业上利用煤的气化产物(水煤气)合成甲醇和二甲醚。回答下列问题:
(1)制备二甲醚最后一步反应由Al2O3催化甲醇脱水合成,反应方程式为 。
(2)已知:CO(g)+2H2(g)=CH3OH (g) △H= —90.1kJ·mol-1
CO(g)的燃烧热是282.8 kJ·mol-1;H2的燃烧热是285.8 kJ·mol-1
写出表示CH3OH (g) 燃烧热的热化学反应方程式 。
(3)二甲醚直接燃料电池比甲醇直接燃料电池更高效,等质量的二甲醚和甲醇完全放电转移电子的物质的量之比是 。用二甲醚直接燃料电池电解足量饱和食盐水,当消耗9.2g二甲醚时理论上阴极产生的气体的体积为 L。(标况下)
(4)在合成中伴有水煤气交换反应:CO(g)+H2O(g)  CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
| 温度 | 260℃ | 280℃ | 295℃ | 310℃ |
| CO转化率 | 89% | 80% | 75% | 60% |
①请解释CO转化率随温度变化的关系 。
②列式计算280℃时平衡常数 。
③若平衡体系中,测得H2的压强占总压的30%,要使体系中CO转化率达到70%,应该使温度 (填“升高”、“降低”、“不变”)
科目:高中化学 来源: 题型:
将容积为50 mL的量筒充满二氧化氮和氧气的混合气体,将量筒倒置在盛满水的水槽里,一段时间后,量筒里剩余气体体积为5 mL。则原混合气体中NO2和O2体积比可能是__________或________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中正确的是( )
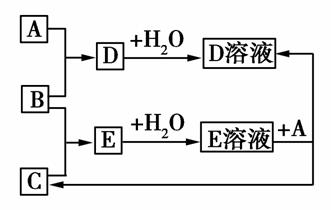
A.A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B.A、B、C中三种元素的任意两种元素形成的化合物所属物质类别一定不是碱
C.如果E溶液是一种强酸,则E溶液为硫酸
D.A、B、C中有一种金属且为B
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在实验室从如图Ⅰ标签的试剂瓶中取少许钠进行燃烧实验(如图Ⅱ)。
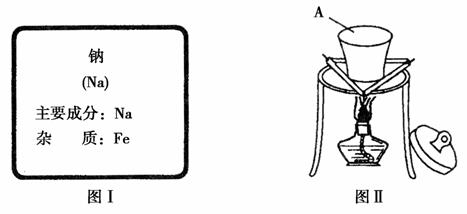
(1)装置A的名称是________;实验中,观察到的淡黄色的固体物质是________(写化学式);观察到黄色火焰是________元素的发射光谱。
(2)实验后发现还有少许黑色固体生成。从反应物及实验操作猜测:该黑色物质可能为碳与另一种氧化物组成的混合物。则该氧化物可能是________或________(写化学式)。
(3)对黑色固体物质的组成作如下探究。
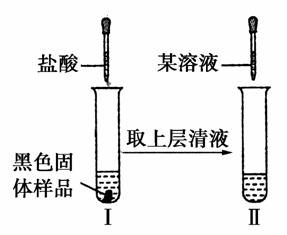
①实验Ⅰ加入盐酸溶液的目的是________。
②仅通过实验Ⅱ,用最简步骤能快速确定黑色物质的组成,请完善该设计。限选试剂:稀盐酸、KSCN溶液、K3[Fe(CN)6]溶液、10%H2O2。
| 实验操作 | 预期的现象与结论 | 相关离子方程式 |
| 取少量实验Ⅰ澄清溶液,加入________ | ________ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1 NaHSO4溶液:K+、Fe2+、NO3-、Cl-
B.0.1 mol·L-1NaAlO2的溶液:K+、Na+、SO42-、CO32-
C.无色溶液:Ba 2+、Na+、MnO4-、NO3-
D.由水电离出的c(OH-)=1.0×10-12 mol·L-1的溶液:NH4+、HCO3-、Na+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
物质A~G是中学化学中常见的物质,这些物质有如图所示的转化关系(部分反应物、生成物没有列出)。其中A、B、F含有一种相同的元素,C、D、G含有一种相同的元素,F具有磁性,G为黑色非金属单质。
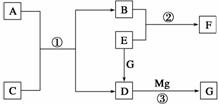
(1)物质A溶解于盐酸,然后加入KSCN溶液,溶液不变色,再滴加几滴氯水,溶液变为血红色,由此推知A的化学式为__________。
(2)反应③的化学方程式是_______________________________________________。
(3)写出下列物质的化学式:E__________、F__________。
(4)若C是一种气体,在温度为1 100 ℃的某固定容积的密闭容器中发生反应:A(s)+C(g)B(s)+D(g) ΔH=a kJ·mol-1(a>0),该温度下平衡常数K=0.263。若生成1 mol B,则吸收的热量________(选填“大于”、“等于”或“小于”)a kJ;若加入过量的A,则C的转化率________(选填“升高”、“不变”或“降低”);若容器内压强不再随时间变化,则该反应__________(选填“达到”、“未达到”或“不一定达到”)化学平衡状态;该反应达到化学平衡状态时,若[C]=0.100 mol·L-1,则[D]=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
某 研究小组提取三处被污染的水源进行了如下分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
研究小组提取三处被污染的水源进行了如下分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO |
为了鉴别上述化合物,分别完成以下实验,其结果是
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)写出D、E发生反应的离子方程式:____________________________________。
(3)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为__________。
(4)C常用作净水剂,用离子方程式表示其净水原理:______ ______________________。
______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中。
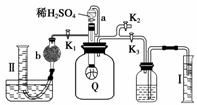
请回答下列问题:
(1)Q内发生反应生成________种气体,其中的反应有________个氧化还原反应。
(2)为测定反应时生成气体的总体积,滴稀H2SO4前必须关闭________(填“K1”、“K2”或“K3”,下同),打开___________________________________________________。
(3)当上述反应停止时,将K1、K2、K3均关闭,然后先打开K2,再缓缓打开K1,这时可观察到的现象是__________________________________________________________。
(4)b中装的固体试剂是__________,请写出缓缓打开K1的理由__________。
(5)实验结束时,量筒Ⅰ中有x mL水,量筒Ⅱ中收集到 y mL 气体,则过氧化钠的纯度是________(用含x、y的式子表示,上述体积均已折算成标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.乙酸乙酯和纤维素乙酸酯均可水解生成乙醇
B.溴乙烷、苯酚一定条件下都能与NaOH水溶液发生反应
C.苯、乙烯都能使酸性KMnO4溶液褪色
D.葡萄糖和蔗糖溶液都能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com