
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(2013?济南一模)下列实验操作及现象能够达到对应实验目的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

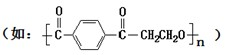 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验 编号 |
T/K | 反应 时间/h |
反应物的物质的量配比 n[CO(NH2)2]:n[MgCl2?6H2O] |
实验目的 |
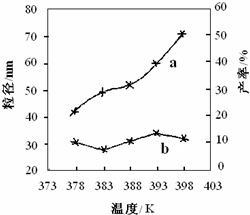
| ① | 378 | 3 | 3:1 | (Ⅰ)实验①和③探究 反应物的物质的量配比对产率的影响 反应物的物质的量配比对产率的影响 删除此空 删除此空 ;(Ⅱ)实验②和④探究 温度对产率的影响 温度对产率的影响 ;(Ⅲ)实验②和 ③ ③ 探究反应时间对产率的影响. |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
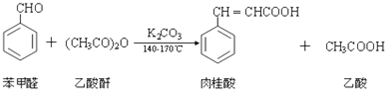
| 名称 | 分子量 | 性状 | 密度g/cm3 | 熔点℃ | 沸点℃ | 溶解度:克/100ml溶剂 | ||
| 水 | 醇 | 醚 | ||||||
| 苯甲醛 | 106 | 无色液体 | 1.06 | -26 | 178-179 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 无色液体 | 1.082 | -73 | 138-140 | 12 | 溶 | 不溶 |
| 肉桂酸 | 148 | 无色结晶 | 1.248 | 133-134 | 300 | 0.04 | 24 | 溶 |
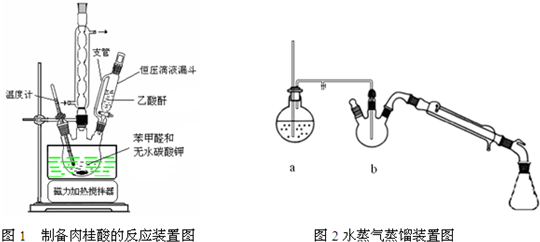
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com