
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 常溫常压下,36g18O2中所含的中子数为16NA
B. 4.6 gNO2与N2O4的混合气体中所含氮原子数为0.1 NA
C. 标准状况下,2.24 L 苯含有的分子数等于0.1 NA
D. 在过氧化钠与水的反应中,每消耗0.1mol过氧化钠,转移电子的数目为0.2 NA
科目:高中化学 来源: 题型:
【题目】Ⅰ.原电池是一类重要的化学电源,请填写下列空白。
(1)将锌片和银片浸入稀H2SO4中组成原电池,两极间连接一个电流计,写出该电池的电极总化学反应方程式为__________。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称量,总质量为47g,则产生标况下的氢气_______升,导线上转移的电子为_____NA。
(3)若12.8g铜与一定量的浓HNO3混合反应,铜耗尽时共产生5.6L(标准状况)NO和NO2的混合气体,则所消耗的HNO3的物质的量为___,混合气体的平均相对分子质量为___。
Ⅱ.现有纯铁片、纯银片、纯铜片、稀硫酸、FeSO4溶液、Fe2(SO4)3溶液,大烧杯、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱。
(1)写出电极反应式,负极:__________,正极__________。
(2)请在下面方框中画出原电池的装置图,要求:注明电解质溶液名称、正负极材料,并标出电子移动方向。
 __________。
__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝、铜三种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有( )
A.AlO2﹣
B.Cu2+
C.Al3+
D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按以下框图进行反应。又知E溶液是无色的,请回答:
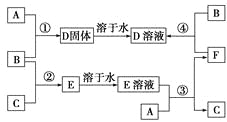
(1)A是________、B是________、C是________(请填化学式)。
(2)反应①的化学方程式为:
________________________________________________________________________。
(3)反应③的化学方程式为:
________________________________________________________________________。
(4)反应④的化学方程式为:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分,将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO2。
猜想2:该气体为SO2。
猜想3:______________________________________________________。
为了验证猜测,该小组设计实验加以探究。
[实验探究]
该小组同学按如图所示装置,将气体从a端通入。
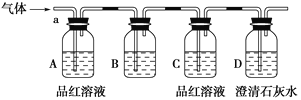
(1)B中应该装下列________试剂(填编号)。
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是________________________________________________。
(3)D中澄清石灰水的作用是______________________________________________。通过该实验,该小组同学观察到以下三个实验现象:①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
[得出结论]
(4)由上述现象,该小组同学确认该气体的成分为:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系,该元素(用R 表示)的单质能与NaOH溶液反应生成盐(Na2RO3)和氢气。

请回答下列问题:
(1)写出各物质的化学式:A________;B________;C________;D________;E________。
(2)写出反应①的化学方程式:______________________________________,该反应中氧化剂与还原剂的物质的量之比为________。
(3)写出反应④的离子方程式:______________________________________。
(4)写出反应⑤的离子方程式:______________________________________。
(5)H2CO3的酸性强于E的,请用离子方程式予以证明:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】易燃易爆、有毒的化学物质在其包装上应贴上危险警告标签。下列物质贴错标签的是( )
选项 | A | B | C | D |
物质的化学式 | 浓H2SO4 | CH3CH2OH | NaOH | NH4NO3 |
危险警告标签 | 腐蚀品 | 易燃品 | 剧毒品 | 爆炸品 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。

实验步骤如下:
①连接好实验装置,检查装置的气密性。
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g。
③加热,开始反应,直到不再有气体产生为止。
④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279. 7 mL。
⑤准确称量试管和残留物的质量为15. 55 g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集的气体体积必须包括的几个步骤:
①调整量筒的高度使广口瓶和量筒内的液面高度相同;
②使试管和广口瓶内气体都冷却至室温;
③读取量筒内液体的体积。
这三步操作的正确顺序是_________________(请填写步骤代号)。
进行③的实验操作时,若仰视读数,则读取氧气的体积_______(填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是_____mol;实验测得氧气的气体摩尔体积是______(保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各问题
(1)泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷守恒__________________;②物料守恒______________________;③质子守恒______________________________;④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com