
某同学想利用图示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物。
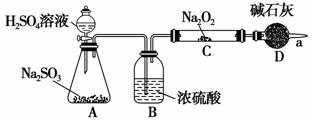
测得反应前C管的质量为m1 g,反应后C管的质量为m2 g,反应后装置D质量增加了n g。请分析:
Ⅰ.装置B的作用_________________________________________________;
装置D的作用_________________________________________________。
Ⅱ.如何检验反应中是否有O2生成______________________________________。
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3,假设2:只有Na2SO4
假设3: ______________________________________________。
(1)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:将C中的固体配成溶液,加Ba(NO3)2溶液,得到白色沉淀,加足量稀硝酸,沉淀不溶解。得出结论:产物是Na2SO4。
该方案是否合理________(填“是”或“否”),理由是__________________________________________________________________
________________________________________________________________________。
(2)若假设1成立,某同学以反应前后C管的质量差(m2-m1)g为依据推断生成Na2SO3的质量为(m2-m1)×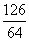 g。老师提示推算不合理,请你分析其中的缘由,________。
g。老师提示推算不合理,请你分析其中的缘由,________。
(3)若假设2成立,则参加反应的Na2O2的物质的量为________mol(列计算式)。
解析 Ⅰ.过氧化钠能与水蒸气反应,装置B的作用就是干燥二氧化硫,装置D的作用是防止空气进入C中。
Ⅱ.检验氧气的方法是用带火星的木条,观察是否复燃。
Ⅲ.假设3为Na2SO3和Na2SO4两者的混合物;
(1)该方案不合理,因为硝酸有氧化性,即使产物为亚硫酸钠,生成的亚硫酸钡也被氧化成硫酸钡;
(2)若假设1成立,则发生反应2Na2O2+2SO2===2Na2SO3+O2,(m2-m1)g不等于参加反应的SO2的质量,故该推算不合理。
(3)若假设2成立,则发生反应Na2O2+SO2===Na2SO4,二氧化硫的质量为(m2-m1)g,n(Na2O2)=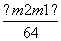 mol。
mol。
答案 Ⅰ.干燥SO2气体,防止水蒸气与Na2O2反应
防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应;同时吸收过量的SO2,以免污染空气
Ⅱ.用带火星的木条靠近干燥管口a,观察其是否复燃
Ⅲ.有Na2SO3和Na2SO4
(1)否 HNO3有氧化性,可将BaSO3氧化为BaSO4,据此不能确定产物是Na2SO3还是Na2SO4或二者兼有
(2)因为该反应中吸收SO2的同时有O2产生,所以(m2-m1)g不等于参加反应的SO2的质量,故该推算不合理
(3)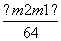


科目:高中化学 来源: 题型:
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O26SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________________________________________________________________________;
从腐蚀废液回收得到金属铜,还需要的试剂是________。
 (3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________________________________________________________________________。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________________________________________________________________________。
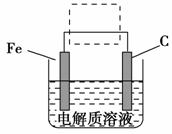
(4)钢铁的电化腐蚀原理如图所示,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在图中虚线框内作出修改,并用箭头标出电子流动方向。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如右图所示。据图判断正确的是( )

A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点Kw的数值比c点Kw的数值大
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关元素性质的说法不正确的是 ( )。
A.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是①
B.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4第一电离能最大的是③
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下图的实验装置用来分离CO2和CO气体并干燥。图中a为止水夹,b为分液漏斗的活塞,通过Y形管和止水夹分别接c、d两球胆,现装置内的空气已排尽。为使实验成功,甲、乙、丙中盛放的溶液分别是( )。

A.NaHCO3饱和溶液、12 mol·L-1盐酸、18.4 mol·L-1硫酸
B.Na2CO3饱和溶液、2 mol·L-1硫酸、NaOH饱和溶液
C.NaOH饱和溶液、2 mol·L-1硫酸、18.4 mol·L-1硫酸
D.18.4 mol·L-1硫酸、NaOH饱和溶液、18.4 mol·L-1硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
有关溶液中所含离子的检验,下列判断中正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO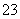 存在
存在
C.用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐酸盐溶液,只用NaOH溶液是不能一次鉴别开的
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要纯净的NaCl溶液,但现有的NaCl晶体混有少量Na2SO4和(NH4)2CO3,请设计实验除去杂质,并回答下列问题:
(1)除去(NH4)2CO3用加热好还是加强碱后再进行加热好?
你选择的是________,其理由是_____________________________。
判断(NH4)2CO3已除尽的方法是_____________________________。
(2)除去SO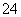 的方法是___________________________________
的方法是___________________________________
________________________________________________________________________。
判断SO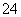 已除尽的方法是______________________________________
已除尽的方法是______________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
三氟化氮(NF3)是微电子工业中一种优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O===2NO+HNO3+9HF,下列有关该反应的说法正确的是( )
A.NF3是氧化剂,H2O是还原剂
B.HF是还原产物
C.还原剂和氧化剂的物质的量之比是2∶1
D.NF3在潮湿的空气中泄漏会产生红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾是一种典型的强氧化剂。
完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①MnO +Cu2S+H+—→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+—→Cu2++SO2↑+Mn2++H2O(未配平)
②MnO +CuS+H+—→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS+H+—→Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是________(填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
(2)标出反应②中电子转移的方向和数目:MnO +CuS
+CuS
Ⅱ.在稀硫酸中,MnO 和H2O2也能发生氧化还原反应
和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为________。由上述反应得出的物质氧化性强弱的结论是________>________(填写化学式)。
(4)已知:2KMnO4+7H2O2+3H2SO4===K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com