
【题目】一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g) ![]() CO2(g)+H2(g),部分数据见下表(表中t2>t1)
CO2(g)+H2(g),部分数据见下表(表中t2>t1)
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
下列说法正确的是
A. 反应在t1min末的速率为v(H2)=0.40/t1 mol·L-1·min-1
B. 平衡时CO的转化率为66.67%
C. 该温度下反应的平衡常数为1
D. 其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.20mol
【答案】C
【解析】t1min末n(CO)=0.8mol,反应消耗n(CO)=0.4mol,根据方程式生成n(CO2)=0.4mol,生成n(H2)= 0.4mol,反应在0--t1min内的平均速率为v(H2)= ![]() 0.20/t1 mol·L-1·min-1,故A错误;t1min末n(CO)=0.8mol,反应消耗n(CO)=0.4mol,消耗n(H2O)=0.4mol,t1min末n(H2O)=0.2mol,t2min末n(H2O)=0.2mol,所以可知t1min末反应达到平衡状态,平衡时CO的转化率为
0.20/t1 mol·L-1·min-1,故A错误;t1min末n(CO)=0.8mol,反应消耗n(CO)=0.4mol,消耗n(H2O)=0.4mol,t1min末n(H2O)=0.2mol,t2min末n(H2O)=0.2mol,所以可知t1min末反应达到平衡状态,平衡时CO的转化率为![]() 33.33%,故B错误;t1min末反应达到平衡状态,n(CO)=0.8mol、n(H2O)=0.2mol、n(CO2)=0.4mol、n(H2)=0.4mol,该温度下反应的平衡常数
33.33%,故B错误;t1min末反应达到平衡状态,n(CO)=0.8mol、n(H2O)=0.2mol、n(CO2)=0.4mol、n(H2)=0.4mol,该温度下反应的平衡常数 ,故C正确;若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.40mol,故D错误。
,故C正确;若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.40mol,故D错误。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程

请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是 __________________________。
(2)氧化池通入Cl2的目的是氧化 _________________________(填化学式),工业上不选用硝酸做氧化剂的原因是_________________和_________________________。
(3)物质甲可以是_____________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 __________________________。
(5)当Fe3+完全沉淀时,求最小pH__________。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g) ![]() 2c(g) △H1<0; x(g)+3y(g)
2c(g) △H1<0; x(g)+3y(g) ![]() 2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是
A. 等压时,通入z气体,反应器中温度升高
B. 等容时,通入z气体,y的物质的量浓度增大
C. 等容时,通入惰性气体,各反应速率不变
D. 等压时,通入惰性气体,c的物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理来解释的是 ( )
A. 用排饱和食盐水的方法收集氯气
B. 合成氨工业选择高温(合成氨反应为放热反应)
C. 增大压强,有利于SO2和O2反应生成SO3
D. 在Fe3++3SCN-![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。
(1)根据下图写出合成氨的热化学方程式是__________________。

(2)将1molN2(g)和3molH2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量____(填“大于”、“等于”或“小于”)92.9KJ,原因是_______;若加入催化剂,△H______(填“变大”、“不变”或“变小”)。
(3)已知分别破坏1molN≡N键、1molH-H键时需要吸收的能量为946KJ、436KJ。则破坏1molN-H键需要吸收的能量为___________KJ。
(4)发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g).
已知N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ/mol;
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol;
写出1mol N2H4与NO2反应的热化学方程式为_______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含1mol HCl和1mol MgSO4的混合溶液中加入1 mo1·L-1Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系如图三其中正确的是
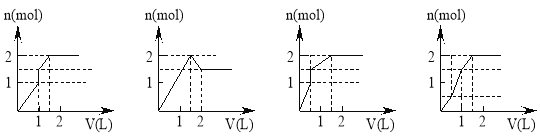
A. B. C. D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com