
【题目】元素单质及其化合物有广泛用途,根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是 。
a.原子序数和离子半径均减小 b.金属性减弱,非金属性增强
c.氧化物对应的水合物碱性减弱,酸性增强 d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是 。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是 ;制铝时,电解Al2O3而不电解AlCl3的原因是 。
(4)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
![]()
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式: 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是 。
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃ 时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式: 。
【答案】(1)b (2)氩 Na+(钠离子)
(3)MgO的熔点高,熔融时耗费更多资源,增加生产成本 AlCl3是共价化合物,熔融态难导电
(4) SiCl4(g)+2H2(g)
SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) H= +0.025 kJmol1
Si(s)+4HCl(g) H= +0.025 kJmol1
(5)b (6)4KClO3 ![]() KCl + 3KClO4
KCl + 3KClO4
【解析】回答本题的要点是:首先熟练掌握元素周期律,如酸碱性和非金属性、原子半径和离子半径的递变规律,根据电子排布和性质推断元素,然后根据分析物质的性质和运用有关化学知识解答本题。
(1)a、原子序数递增,离子半径也可能增大,错误;b、第三周期随原子序数的递增,金属性减弱,非金属性增强,增强;c、没有指明为最高价氧化物,错误;d、单质的熔点也可能增大,错误。
(2)第三周期原子最外层电子数与次外层电子数相同的元素是氩,都是8;氧化性最弱的是简单阳离子是Na的阳离子,Na+
(3)MgO的熔点远远大于MgCl2的熔点,熔融时耗费更多资源,增加生产成本;AlCl3是共价化合物,熔融态难导电,所以不能电解熔融AlCl3。
(4)SiCl4中Si分别与Cl形成1对共用电子,所以电子式为:
生成1.12kg纯硅需吸收akJ热量,则生成28g纯硅需吸收0.025 kJ,可得热化学方程式。
(5)NH3既不能用浓硫酸干燥,也不能用P2O5干燥,HI不能用浓硫酸干燥,可用P2O5干燥,SO2不能用浓硫酸干燥,CO2能用浓硫酸干燥,所以b项正确。
(6)一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,根据氧化还原反应原理,这两种盐为KCl、KClO4,配平可得化学方程式。


科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.NaHS水解反应:HS-+H2O![]() H3O++S2-
H3O++S2-
B.明矾加入在水中起净化作用的原因:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
C.氢氧化钡溶液与稀硫酸反应:![]()
D.碳酸氢钠溶液中加入过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有SO42-、CO32-、Cl-。为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( )
A. H2SO4溶液 B. HCl溶液
C. NaOH溶液 D. NaNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的名称是______,碱性最强的化合物的化学式是_______。
(2)⑤⑦形成化合物的电子式___。②形成的最高价氧化物的结构式____。
(3)最高价氧化物是两性氧化物的元素其元素符号是____;写出它的氢氧化物与⑧的最高价氧化物的水化物反应的离子方程式________。
(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是______。
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL BaCl2、AlCl3、FeCl3的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如下图所示:
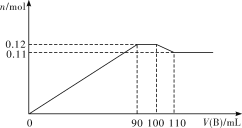
(1)当加入110 mL B溶液时,溶液中的沉淀是___________(填化学式)。
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是___________。当B溶液加到90 mL~100 mL这一段时间中,所发生的离子反应方程式是____________________。
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中。
溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
c/mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修5:有机化学基础]有机物G(![]() )是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
)是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:

(1)A与银氨溶液反应有银镜生成,则A的结构简式是____________,D中官能团名称为_________________B→C的反应类型是________反应。
(2)下列关于G的说法不正确的是__________(填字母)。
A.能与溴的四氯化碳溶液反应 b.能与金属钠反应
C.1molG最多能和5mol氢气反应 d.分子式是C9H6O3
(3)写出一种满足下列条件的E的同分异构体的结构简式:___________________。
①苯环上的一氯取代产物只有两种;
②能发生银镜反应;
③能与FeCl3溶液发生显色反应。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:_____________。
(5)请设计合理的方案以苯酚和乙醇为原料合成乙酸苯酯(![]() )(用合成路线流程图表示,并注明反应条件)。提示:①合成过程中无机试剂任选;②合成反应流程图表示方法示例如下:A
)(用合成路线流程图表示,并注明反应条件)。提示:①合成过程中无机试剂任选;②合成反应流程图表示方法示例如下:A![]() B
B![]() C……→D。
C……→D。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O)
C. 3v(NH3)=2v(H2O) D. 5v(O2)=4v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
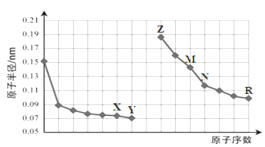
A. X与M形成的一个阴离子中含有29个电子
B. 气态氢化物沸点Y>R
C. 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z单质能从M与R元素构成的盐溶液中置换出单质M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com