
【题目】某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
A. 平衡向正方向移动 B. 平衡不发生移动
C. C的体积分数减小 D. C的体积分数不变
科目:高中化学 来源: 题型:
【题目】有A、B和C三种主族元素,若A元素阴离子与B、C元素的阳离子具有相同的电子层结构,且B的阳离子半径大于C,则这三种元素的原子序数大小次序是( )
A. A<B<C B. B<C<A C. C<B<A D. A<C<B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 氮原子的价电子排布图:![]()
B. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
C. 2p和3p轨道形状均为哑铃形,能量也相等
D. 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为元素周期表前四周期的元素。其中X是形成化合物种类最多的元素,Y的内层电子数是最外层电子数的9倍,Z是元素周期表中电负性最大的元素,W元素的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题。
(1)W元素在元素周期表中的位置为______________________________。
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。写出该配离子的结构简式(标明配位键)_______。
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为__________,1mol该分子中σ键的数目为______________,该物质易溶于水的主要原因是________________。
(4)X的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为______________________。
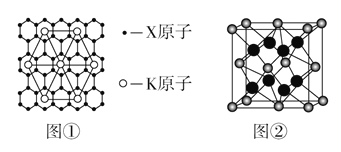
(5)元素Y与元素Z形成的晶胞结构如图②所示,该晶胞中Y离子周围最近的Z的离子为___个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质]
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4。回答下列问题:
⑴写出基态Zn原子的价电子排布式__________,基态S原子核外未成对电子数为_____。
⑵ZnSO4中三种元素的电负性由大到小的顺序为_____________________,SO42-的立体构型为________________,其中S的杂化轨道类型为_________。
⑶硫酸锌溶于氨水可生成[Zn(NH3)4]SO4溶液,[Zn(NH3)4]SO4溶液中不存在的微粒间作用力有___________。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
⑷根据下列锌卤化物的熔点和溶解性,判断ZnF2晶体的类型为___________;分析ZnCl2、ZnBr2、ZnI2熔点依次增大的原因________________。
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
⑸立方ZnS晶体的密度为ρg·cm-3,其晶胞结构如图。S2-周围等距离且最近的Zn2+、S2-依次为______、______;ZnS晶胞中的晶胞参数a=________nm(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含有MgO、SiO2等杂质]为原料,制备金属钛和铁红的工艺流程如下:

已知:①酸酸时,FeTiO3转化为Fe2+和TiO2+ ;
②本实验温度下,Ksp[Mg(OH)2]=1.0×10-11;
③溶液中离子浓度小于等于l .0×10-5mol/L时,认为该离子沉淀完全。
请国答下列问题:
(1)FeTiO3中Ti元素的化合价为_____价,铁红的用途为_____(任写一种)。
(2)“水解”中,发生反应的离子方程式为________。
(3)“沉铁”中,气态产物的电子式为______;该过程需控制反应温度低于35 ℃,原因为_______。
(4)FeCO3转化为铁红时,发生反应的化学方程式为____________。
(5)滤液3可用于制备Mg(OH)2。若滤液3中c(Mg2+)=1.2×10-3mol/L,向其中加入等体积的NaOH溶液的浓度为________ mol/L时,可使Mg2+恰好沉淀完全(溶液体积变化忽略不计)。
(6)“电解”时,电解质为熔融的CaO,则阴极反应式为_______,制得1molTi单质,理论上导线中通过的电量为______(保留三位有效数字,已知:l 个电子的电量为1.6×10-19C ) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的有

A. 在H3BO3分子中各原子最外层全部满足8电子稳定结构
B. H3BO3分子的稳定性与氢键有关
C. 1mol H3BO3的晶体中有3mol极性共价键
D. 1mol H3BO3的晶体中有3mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结构为…—CH=CH—CH=CH—CH=CH—CH=CH-…的高分子化合物用碘蒸气处理后,其导电能力大幅度提高。上述高分子化合物的单体是
A.乙炔 B.乙烯 C.丙烯 D.1,3-丁二烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com