
【题目】若短周期的两元素可形成原子个数比为2∶3的化合物,则这两种元素的原子序数之差不可能是( )。
A. 6 B. 3 C. 5 D. 1
科目:高中化学 来源: 题型:
【题目】在两个密闭容器甲、乙中,依次充入氧原子数目相同的O2、O3两种气体,若它们的温度和密度均相同。下列说法正确的是
A. 气体体积:甲>乙 B. 气体的质量:甲<乙
C. 气体的分子数:甲<乙 D. 气体的压强:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯氧化法制备苯甲酸的反应原理如下:
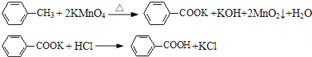
实验时将一定量的甲苯和KMnO4溶液置于图装置中,在100 ℃时,反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。
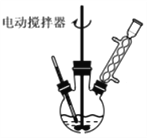
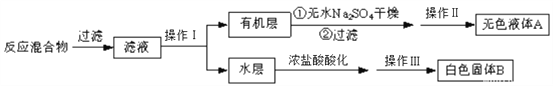
(1)反应图示装置中,冷凝管的作用是________。
(2)实验室中实现操作I所需的玻璃仪器有_________,烧杯;操作II的名称为_______。
(3)如果操作I后的水层呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,否则会出现的危害是______。
(4)分离出的苯甲酸中若混有少量氯化钾,进一步提纯应采用的操作方法是_______(填名称)。
(5)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的化学方程式或离子方程式中不正确的是
A. 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH—=SiO32—+H2O
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2H++2I—+H2O2=I2+2H2O
C. 燃煤时加入适量石灰石粉末,可减少SO2的排放:2CaCO3+2SO2+O2![]() 2CaSO4+2CO2
2CaSO4+2CO2
D. 强碱溶液中,用次氯酸钠与Fe(OH)2反应制备高铁酸钠:2ClO—+ Fe(OH)2=FeO42—+2Cl—+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质灼烧时焰色反应为黄色,则下列判断正确的是( )
A.该物质一定是金属钠B.该物质一定是氯化钠
C.该物质一定是钠的化合物D.该物质一定含钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D,E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
A. BADCE B. ECDBA C. ABCDE D. CDABE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其元素特征信息如下表。回答下列问题:

(1)写出下列元素的符号:A:________,E:________;
(2)写出C与B 形成的两种离子化合物的化学式_______;______。
(3)指出 E 在周期表中的位置 _____________。
(4)B、C、D三种元素的离子半径由大到小的顺序是_________(写具体的元素符号)。
(5)E单质和C的最高价氧化物对应水化物水溶液反应的离子方程式:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com