
已知:①A的简单阴离子核外有2个电子,B元素原子最外层电子数是内层电子数的3倍,E原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于分子晶体,F元素原子序数为26。
②X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:

回答下列问题:
(1)B元素原子核外已成对电子数是未成对电子数的____倍。
(2)X、Y、Z的电负性从大到小的顺序为____(用元素符号表示)。
(3)分子式为A2B、A2E的两种物质中 __更稳定(用化学式表示),原因是____。
(4)X的氯化物的熔点比Y的氯化物的熔点____,原因是____。
(5)F的氯化物FCl3与KSCN溶液反应显红色,该反应的离子方程式为____。等电子体指的是原子总数相同.价电子总数相同的分子.离子或基团,据此定义写出离子SCN—的一种等电子体____。
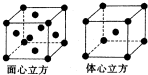
(6)F的一种常见配合物F(CO)3常温下呈液态,熔点为- 20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断F(CO)5的晶体类型为 。F元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如
图所示。在面心立方晶胞中F原子的配位数为____,体心立方晶胞的密度可表示为____。(F的原子半径为r)

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| A | A的基态原子最外层电子排布式为2S22P3 |
| B | B是地壳中含量最高的元素 |
| C | C+与B的简单离子的电子层结构相同 |
| D | D的一种核素的质量数为64,中子数为35 |
| E、F | E、F既同周期又同族,且原子序数F比E多2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业 高一化学(下) 题型:022
A、B、C、D为原子序数小于18的四种元素.已知:A的原子的电子层数等于最外层电子数,A与B同一周期,B与D可形成离子化合物 ,该化合物的水溶液呈碱性,C的离子核内质子数与核外电子数之和为18,A、C、D三元素的简单离子具有相同的电子层排布,填空:
,该化合物的水溶液呈碱性,C的离子核内质子数与核外电子数之和为18,A、C、D三元素的简单离子具有相同的电子层排布,填空:
(1)A、B、C、D各为何种元素?(填元素符号)
A.________
B.________
C.________
D.________
(2)四种元素的离子半径大小顺序为:________
(3)用电子式表示 的形成过程:________
的形成过程:________
(4)用离子方程式表示 的水溶液和盐酸反应的过程:________
的水溶液和盐酸反应的过程:________
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、和D都是周期表中前20号元素,已知:
①A的阳离子D的阴离子具有相同的核外电子排布,且能形成组成为AD的化合物;
②B和D属同族元素,它们能形成两种常见化合物;
③C和B属同一周期元素,它们能形成两种气态化合物:
④C和B、D和B、A和C、C和D都能形成组成为WX2型的化合物;
⑤它们形成WX2型的化合物中有一种是实验室制取某种气体的原料,有一种是有机溶剂。
请回答:
(1)化合物AD和AC2的化学式分别是 和 。
(2)写出实验室以AC2为原料制取气体的化学方式 。
(3)B和D形成的两种常见化合物的分子式是 和 。
(4)写出D和B形成的一种气态化合物跟AB反应的化学方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com