
电解饱和食盐水制得H2、Cl2、NaOH(氯碱工业).
电极反应:阳极(石墨):________;
阴极(铁棒):________;
总反应:________.
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
 工业上电解饱和食盐水可得到多种工业原料,其中氢气和氯气用途非常广泛.
工业上电解饱和食盐水可得到多种工业原料,其中氢气和氯气用途非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |
| 预期产物的相对分子质量 |
| 全部生成物质的相对分子质量总和 |
| a1V2 |
| 4a2(1-a1) |
| a1V2 |
| 4a2(1-a1) |
| 23V |
| 134.4 |
| 23V |
| 134.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
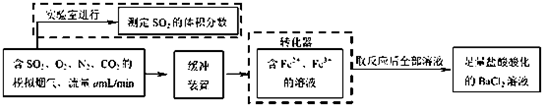
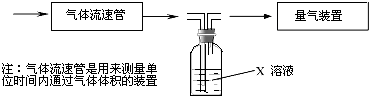
科目:高中化学 来源: 题型:阅读理解
| 1 |
| x |
| 1 |
| x |
| 3 |
| x |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省高三上学期第二次阶段性测试化学试卷 题型:填空题
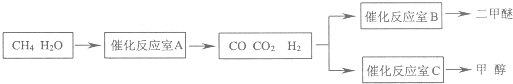
(11分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链,大大地提高了资源利用率,减少了环境污染。其流程如下:
请回答下列问题:
(1)由CO和H2合成甲醇的化学方程式是CO(g)+2H2(g) CH3O(H(g)。若在恒容密 闭容器中充入一定量的CO和H2,在一定条件下反应,能说明该反应已达到平衡状态的是
CH3O(H(g)。若在恒容密 闭容器中充入一定量的CO和H2,在一定条件下反应,能说明该反应已达到平衡状态的是
(填字母)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(CO)=c(CH3OH) d.V正(CO)=v逆(CH3OH)
(2)写出流程中氯化时发生反应的化学方程式: 。
(3)20℃时,电解饱和食盐水制得烧碱的混合液中,随着NaOH含量的变化,NaCl达到饱和状态时其溶质质量分数的变化曲线如图所示。现有20℃时,满足曲线上B点所示的溶液,要降低溶液中NaCl的含量,可采用的方法是 。若向B点所示溶液中通入Cl2至恰好呈中性,此时溶液中各离子浓度从大到小的顺序为 。
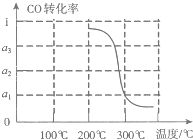
(4)在某次联合生产过程中,氯碱厂电解电路中通过了20mol电子,同时甲醇厂获得了147.2g甲醇,则理论上冶钛厂可得钛 g(精确到0.1,下同),甲醇厂CO的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com