
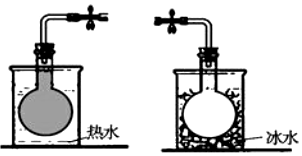
 在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )
在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )| A. | 该反应的正反应为吸热反应 | |
| B. | 反应达到平衡时,再充入少量NO2,平衡后NO2的转化率增大 | |
| C. | 反应达到平衡时,再充入少量N2O4,气体颜色变浅 | |
| D. | 反应达到平衡时,增大压强,平衡向正反应方向移动,逆反应速率减小 |
分析 A.由图可知,温度高颜色深,则升高温度,2NO2?N2O4逆向移动;
B.该反应为气体体积减小的反应,再充入少量NO2,平衡正向移动;
C.反应达到平衡时,再充入少量N2O4,平衡时NO2的浓度比原平衡时浓度大;
D.增大压强,正逆反应速率均增大.
解答 解:A.由图可知,温度高颜色深,则升高温度,2NO2?N2O4逆向移动,则正反应为放热反应,故A错误;
B.该反应为气体体积减小的反应,再充入少量NO2,平衡正向移动,则平衡后NO2的转化率增大,故B正确;
C.反应达到平衡时,再充入少量N2O4,平衡时NO2的浓度比原平衡时浓度大,则颜色比原平衡时深,故C错误;
D.增大压强,正逆反应速率均增大,且正向移动,故D错误;
故选B.
点评 本题考查化学平衡的影响因素,为高频考点,把握温度、浓度、压强对反应速率及平衡的影响为解答的关键,侧重分析与应用能力的考查,注意反应的特点及选项C为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 贮氢金属并不是简单地吸附氢气,而是通过化学反应贮存氢气 | |
| B. | 物质变化中炭化、钝化、皂化、酯化、熔化都属于化学变化 | |
| C. | 石油分馏的馏分之一是石油气,石油气含有大量的己烷 | |
| D. | 使用煤液化的产品作燃料与直接燃烧煤比较,对保护环境有利,目前,煤液化的唯一途径是将煤在高温和催化剂条件下与氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
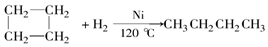
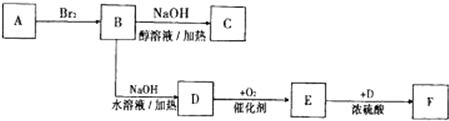
 ;C
;C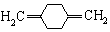 ;
;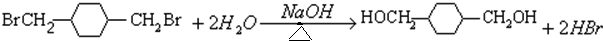 ;E→F:
;E→F: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加反应的Fe2+全部作还原剂 | |
| B. | 生成1.5molFe3O4时,反应转移电子 6mol电子 | |
| C. | 方程式中a=2 | |
| D. | 反应中被氧化的元素是Fe,被还原的元素是S和O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤①③②④ | B. | ④②③①⑤ | C. | ①⑤③②④ | D. | ①⑤③④② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实际应用 | 化学原因 | |
| A | “84”消毒液和洁厕灵不能混合使用 | 发生化学反应产生有毒气体 |
| B | FeCl3腐蚀Cu刻制印刷电路板 | 铁比铜金属性强 |
| C | 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 | 酸、碱还有盐可直接侵蚀铝的保护膜以及铝制品本身 |
| D | 明矾、硫酸铁可作净水剂 | 溶于水形成胶体从而凝聚水中的悬浮物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Fe3+、Cu2+ | B. | Fe2+、Cu2+、Fe3+ | C. | Cu2+、Fe2+、Fe3+ | D. | Fe3+、Cu2+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4Cl受热易分解,可用作氮肥 | |
| C. | MgO熔点高,可用作耐高温材料 | |
| D. | KAl(SO4)2•12H2O易溶于水,可用作净水剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com