
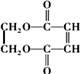
 的合成路线如图:
的合成路线如图: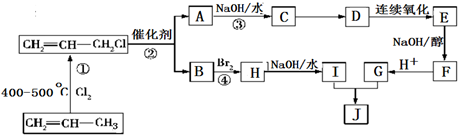
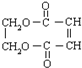 .
.分析 丙烯在加热条件下和氯气发生加成反应生成CH2=CHCH2Cl,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2;B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH;A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,由J的结构可知,G为HOOC-CH=CH-COOH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为HOOCCH2CH(Cl)COOH,据此分析解答.
解答 解:丙烯在加热条件下和氯气发生加成反应生成CH2=CHCH2Cl,CH2=CHCH2Cl在催化剂条件下生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2;B与溴发生加成反应生成H,H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I,I为HOCH2-CH2OH;A在氢氧化钠水溶液、加热条件下发生反应生成C,C为HOCH2CH=CHCH2OH,C生成D是C与HCl的加成反应,故D为HOCH2CH2CHClCH2OH,由J的结构可知,G为HOOC-CH=CH-COOH,E发生消去反应生成F,F酸化得到G,故F为NaOOC-CH=CH-COONa,E为HOOCCH2CH(Cl)COOH,
(1)通过以上分析知,B为CH2=CH2,名称是乙烯,故答案为:乙烯;
(2)A为ClCH2CH=CHCH2Cl,卤代烃和NaOH的水溶液发生水解反应生成醇,该反应的反应方程式为ClCH2CH=CHCH2Cl+2NaOH$→_{△}^{H_{2}O}$HOCH2CH=CHCH2OH+2NaCl,
故答案为:ClCH2CH=CHCH2Cl+2NaOH$→_{△}^{H_{2}O}$HOCH2CH=CHCH2OH+2NaCl;
(3)E为HOOCCH2CH(Cl)COOH、G为HOOC-CH=CH-COOH,G中官能团名称是羧基和碳碳双键,
故答案为:HOOCCH2CH(Cl)COOH;碳碳双键和羧基;
(4)HOCH2-CH2OH和HOOC-CH=CH-COOH在浓硫酸加热的条件下发生酯化反应,生成环酯,反应方程式为HOCH2-CH2OH+HOOC-CH=CH-COOH$→_{△}^{浓硫酸}$2H2O+ ,
,
故答案为:HOCH2-CH2OH+HOOC-CH=CH-COOH$→_{△}^{浓硫酸}$2H2O+ ;
;
(5)D为HOCH2CH2CHClCH2OH,D的同分异构体中Cl原子位于端头碳原子上,且2个羟基不在同一个碳原子上的有ClCH2CHOHCH2CH2OH、ClCH2CH2CHOHCH2OH、ClCHOHCH2CH2CH2OH、ClCH2CHOHCHOHCH3、ClCHOHCH2CHOHCH3、ClCHOHCHOHCH2CH3、ClCHOHCOH(CH3)2、ClCHOHCH(CH3)CH2OH、ClCH2COH(CH3)CH2OH、ClCH2CH(CH2OH)2,共10种,其中核磁共振氢谱为4组峰,且峰面积比为4:2:2:1的为 ClCH2CH(CH2OH)2,
故答案为:10;ClCH2CH(CH2OH)2.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力及知识获取运用及解答问题能力,正确推断各物质结构简式是解本题关键,涉及同分异构体种类判断、化学方程式的书写、官能团名称判断等知识点,熟练掌握常见有机物官能团及其性质关系、同分异构体种类判断方法,题目难度中等.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | X原子的电子层数比Y原子的电子层数多 | |
| B. | Y的单质能将X从NaX的溶液中置换出来 | |
| C. | X的单质比Y的单质更容易与氢气反应 | |
| D. | X的氢化物水溶液的酸性一定比Y的氢化物水溶液的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
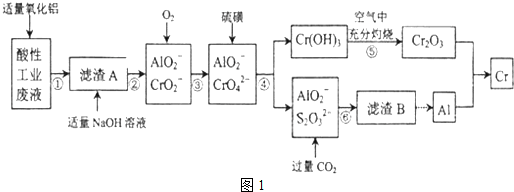
| 化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| 完全沉淀的PH | 10.5 | 4.3 | 5.3 |
| 开始溶解的pH | -- | 7.8 | 9.2 |
| Ksp近似值 | 10-12 | 10-14 | 10-31 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A3B | B. | A3B2 | C. | AB3 | D. | A2B3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 |
| X | 地壳中含量最高的非金属元素 |
| Y | M层比K层多1个电子 |
| Z | 最外层电子数为内层电子数的0.6倍 |
| W | 与氯形成的氯化物是生活中常用的调味品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
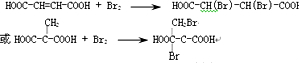
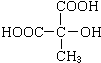 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com