
【题目】已知五种短周期元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成的离子化合物A2B中,所有离子的电子数都相等,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)写出五种元素的名称:A__________,B__________,C________,D________,E________。
(2)用电子式表示离子化合物A2B的形成过程______________________
(3)写出D元素形成的单质的电子式____________。
(4)写出下列物质的电子式:B与E形成的化合物____;A、B、E形成的化合物________;D、E形成的4核10电子化合物__________________。
【答案】钠 氧 硫 氮 氢 ![]()
![]()
![]()
![]()
![]()
【解析】
五种短周期元素的原子序数的大小顺序为C>A>B>D>E。A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30,则离子含有的电子数为10,由A2B可知,A离子为+1价离子,B离子为-2价离子,则A为钠元素,B为氧元素;B、C同主族,则C为硫元素;D和E可形成四核10电子分子,则D为氮元素,E为氢元素。
(1)由分析可知:A为钠元素,B为氧元素,C为硫元素,D为氮元素,E为氢元素。
故答案为: A. 钠 B. 氧 C. 硫 D. 氮 E. 氢
(2)钠原子最外层一个电子,氧最外层6个电子,钠子形成两个离子键,用电子式表示离子化合物Na2O的形成过程![]() ,故答案为:
,故答案为:![]() ;
;
(3)D为氮元素,单质中氮原子之间形成3对共用电子对,D元素形成的单质的电子式![]() ,故答案为:
,故答案为:![]() ;
;
(4)B与E形成的化合物可能为H2O2,氢原子与氧原子之间形成1对共用电子对,氧原子与氧原子之间形成1对共用电子对,电子式为![]() ,也可能形成水,电子式为:
,也可能形成水,电子式为:![]() ;A、B、E形成的化合物为NaOH,属于离子化合物,由钠离子与氢氧根离子构成,电子式为:
;A、B、E形成的化合物为NaOH,属于离子化合物,由钠离子与氢氧根离子构成,电子式为:![]() ;D、E形成的4核10电子化合物为NH3,氮原子与氢原子之间形成1对共用电子对,电子式为:
;D、E形成的4核10电子化合物为NH3,氮原子与氢原子之间形成1对共用电子对,电子式为:![]() 。故答案为:
。故答案为:![]() ;
;![]() ;
; ![]() 。
。


科目:高中化学 来源: 题型:
【题目】我国“神舟七号”载人飞船的火箭燃料主要是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4═3N2+4H2O+2CO2,下列叙述错误的是
A.此反应是氧化还原反应
B.R的分子式为C2H8N2
C.在反应中N2O4做还原剂
D.生成3mol N2时电子转移数为16mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如图:

操作Ⅱ发生反应的离子方程式为___;如果用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,则生成物中溴的化合价分别为+5和﹣1价,且操作Ⅲ中用稀硫酸代替氯气,请写出这种情况下操作Ⅲ中发生反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷高温裂解的产物有甲烷、乙烷、乙烯、丙烯 4 种气体,当丁烷完全分解时,所得裂解气的平均式量为 ( )
A.58B.43.5C.29D.14.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用________,要使MgSO4完全转化为沉淀,加入试剂的量应为________________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_____________。
(3)试剂②选用________;写出其反应的离子方程式_______。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知所用火箭推进剂为肼(N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。请回答下列问题:
(1)NH3、H2O2分子中电负性最大的元素在周期表中的位置为___,第一电离能最大的元素为___。
(2)铬的原子序数为24,其基态电子排布式为___。
(3)1molN2H4分子中含有的σ键数目为___。
(4)H2O2分子结构如图1,其中心原子杂化轨道类型为___,估计它难溶于CS2,简要说明原因___。
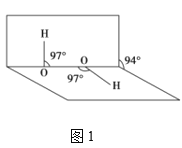
(5)氮化硼晶胞如图2所示,处于晶胞顶点上的原子的配位数为___,若立方氮化硼的密度为ρgcm-3,阿伏加德罗常数为NA,则两个最近N原子间的距离为___cm。
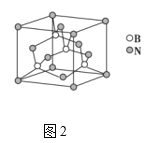
(6)如图3所示,若将A离子移到晶胞的体心,则B离子移到了___(填顶点,面心或棱心)。
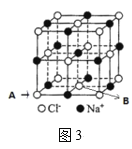
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实:
(1)X+Y2+=X2++Y;(2)Z+2H2O![]() Z(OH)2+H2↑;(3)Z2+离子的放电能力比X2+弱;(4)由Y、W 作电极组成的原电池反应为:Y-2e-=Y2+,由此可知,X、Y、Z、W的还原性由强到弱的顺序是
Z(OH)2+H2↑;(3)Z2+离子的放电能力比X2+弱;(4)由Y、W 作电极组成的原电池反应为:Y-2e-=Y2+,由此可知,X、Y、Z、W的还原性由强到弱的顺序是
A. X > Y > Z > WB. Y > X > W > Z
C. Z > X > Y > WD. Z > Y > X > W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列

表述中正确的是
A.反应的化学方程式为2X = 3Y + Z
B.t时,正、逆反应都不再继续进行,反应达到化学平衡
C.若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D.温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )
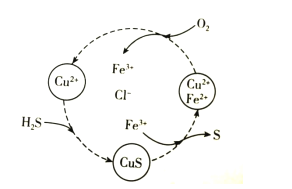
A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2H2S+O2![]() 2S+2H2O
2S+2H2O
D.当有1molH2S转化为硫单质时,需要消耗O2的物质的量为0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com