
| A. | 稀硫酸与氢氧化钡溶液反应:SO42-+Ba2+═Ba SO4↓ | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 石灰石溶于稀盐酸:CO32-+2H+=+CO2↑+H2O | |
| D. | 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
分析 A.该反应漏掉了氢离子与氢氧根离子生成水的反应;
B.铁与稀硫酸反应生成硫酸亚铁和氢气,不是生成亚铁离子;
C.碳酸钙为难溶物,离子方程式中不能拆开;
D.铁与氯化铜溶液反应生成氯化亚铁和铜.
解答 解:A.硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.稀H2SO4与铁粉反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+=Fe2++H2↑,故B错误;
C.碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故C错误;
D.氯化铜溶液与铁粉反应生成氯化亚铁和铜,反应的离子方程式为:Cu2++Fe=Fe2++Cu,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:解答题
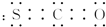 ,其分子呈直线形.
,其分子呈直线形. .
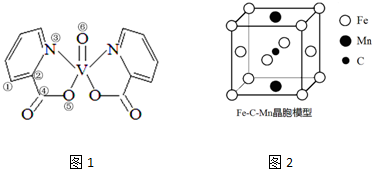
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子层序数越大,s原子轨道的形状相同,半径越大 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,释放能量,由基态转化成激发态 | |
| D. | 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学研究会造成严重的环境污染,最终人类会毁灭在化学物质中 | |
| B. | 化学研究的主要目的是认识分子 | |
| C. | 化学家可以制造出自然界中不存在的物质 | |
| D. | 俄国化学家门捷列夫提出了原子学说,为近代化学的发展奠定了基础 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体与溶液的本质区别是丁达尔效应 | |
| B. | 氯化铁溶液可应急止血,利用的是胶体的聚沉 | |
| C. | 用一束平行光线入射淀粉溶液里,从侧面可以观察到一条光亮的通路 | |
| D. | 将稀硫酸逐滴加入氢氧化铁胶体中,开始时产生沉淀,继续滴加时沉淀又溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据要求回答下列有关问题:
根据要求回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2++2OH-=Cu(OH)2↓CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2OBaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓Ca(NO3)2+Na2CO3═CaCO3↓+NaNO3 | |
| D. | H++OH-=H2OBa(OH)2+H2SO4═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 离子半径:C>D>A>B | B. | 核电核数:b>a>d>c | ||
| C. | 原子半径:A>B>D>C | D. | 元素的电负性:A>B>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L氧气中,一定含有2 mol氧原子 | |
| B. | 80 g NaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L | |
| C. | 18 g水在标准状况下的体积约为22.4 L | |
| D. | 标准状况下,20 mL NH3跟60 mL O2所含分子个数比为1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com