
【题目】香花石由前20号元素中的6种组成,其化学式为![]() ,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
A.原子半径:![]()
B.气态氢化物的稳定性:![]()
C.最高价氧化物对应的水化物碱性:![]()
D.![]() 、
、![]() 两化合物中R的化合价相同
两化合物中R的化合价相同
【答案】D
【解析】
根据T无正价,则T为氟元素;Y、Z、R、T位于同周期,则它们在第二周期,由R最外层电子数为次外层的3倍,则R为氧元素;Z的最外层电子数与次外层相等,则Z为铍元素;Y、Z为金属元素,Y在第二周期,则Y为锂元素;X、Z位于同主族,则X为镁元素或钙元素;若X为镁元素,则由X与R原子序数之和是W的2倍,则![]() ,推出W为氖元素,稀有气体元素化学性质稳定,一般不与其它元素形成化合物,则不符合题意,若X为钙元素,则由X与R原子序数之和是W的2倍,
,推出W为氖元素,稀有气体元素化学性质稳定,一般不与其它元素形成化合物,则不符合题意,若X为钙元素,则由X与R原子序数之和是W的2倍,![]() ,推出W为硅元素,符合题意,即X为钙元素、Y为锂元素、Z为铍元素、R为氧元素、W为硅元素、T为氟元素,据此分析解答。
,推出W为硅元素,符合题意,即X为钙元素、Y为锂元素、Z为铍元素、R为氧元素、W为硅元素、T为氟元素,据此分析解答。
由以上分析知,X为钙元素、Y为锂元素、Z为铍元素、R为氧元素、W为硅元素、T为氟元素,
A. Y为锂元素、Z为铍元素、R为氧元素、T为氟元素,它们位于同周期,元素的原子半径从左向右依次减小,故A正确;
B. W为硅元素、R为氧元素、T为氟元素,非金属性![]() ,非金属元素的非金属性越强,其气态氢化物越稳定,则气态氢化物的稳定性
,非金属元素的非金属性越强,其气态氢化物越稳定,则气态氢化物的稳定性![]() ,故B正确;
,故B正确;
C. X为钙元素、Z为铍元素,金属性Ca>Be,金属元素的金属性越强,其最高价氧化物对应的水化物的碱性越强,则最高价氧化物对应的水化物碱性![]() ,故C正确;
,故C正确;
D. ![]() 、
、![]() 两化合物分别为
两化合物分别为![]() 、
、![]() ,因钙元素为
,因钙元素为![]() 价、硅元素为
价、硅元素为![]() 价,则
价,则![]() 、
、![]() 两化合物中R的化合价分别为
两化合物中R的化合价分别为![]() 、
、![]() 价,故D错误;
价,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】某温度下的密闭容器中发生如下反应:2M(g)+N(g)![]() 2E(g)。若开始时只充入2 mol E(g),达到化学平衡时,混合气体的压强比开始时增大了20%;若开始时只充入2 mol M(g)和1 mol N(g) 的混合气体,则达到化学平衡时M的转化率是
2E(g)。若开始时只充入2 mol E(g),达到化学平衡时,混合气体的压强比开始时增大了20%;若开始时只充入2 mol M(g)和1 mol N(g) 的混合气体,则达到化学平衡时M的转化率是
A. 20% B. 40%
C. 80% D. 60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是一种古老而又年轻的金属元素,铜及其化合物在生产生活中有着广泛的应用。
(1)古代留下来的青铜器表面呈绿色,原因是在潮湿的空气中,铜易发生腐蚀生成铜绿,有关反应的化学方程式为______。
(2)现代工业主要采用高温冶炼黄铜矿![]() ,也可表示为
,也可表示为![]() 的方法获得铜。火法炼铜首先要焙烧黄铜矿:
的方法获得铜。火法炼铜首先要焙烧黄铜矿:![]() ,每转移0.6mol电子,有______mol硫原子被氧化。写出火法炼铜由
,每转移0.6mol电子,有______mol硫原子被氧化。写出火法炼铜由![]() 得到Cu的总方程式______。
得到Cu的总方程式______。
(3)![]() 可用于游泳池水的消毒,原因是______。
可用于游泳池水的消毒,原因是______。
(4)向![]() 和
和![]() 的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为______(已知
的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为______(已知![]() ,
,![]() )。
)。
(5)利用Cu和![]() 溶液的反应可制作印刷线路板,为了从含有
溶液的反应可制作印刷线路板,为了从含有![]() 、
、![]() 、
、![]() 的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
方案1:向废液中加入过量铁粉,充分反应后过滤。在所得滤渣中加入足量盐酸,充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为______。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时Cu已全部析出,在电极上可直接回收铜。操作比方案1简便,但方案2也有不足之处,主要表现为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有机物命名:
![]() ________________________________;
________________________________;
![]() ___________________________________;
___________________________________;
(2)依据名称写出物质:
3,4-二甲基-4-乙基庚烷 ______________;3,4,4-三甲基-1-戊炔 ______________。
(3)已知有机物降冰片二烯的分子结构可表示为: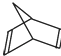
①降冰片二烯的分子式为 ______________;②降冰片二烯属于 __________;
a.环烃 b.不饱和烃 c.烷烃 d.烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)![]() H2(g)+CO(g) ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1,
H2(g)+CO(g) ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1,
①该反应在低温下___________(填“能”或“不能”)自发进行。
②写出该反应的平衡常数表达式_________________。
(2)已知在400℃时,N2(g)+3H2(g)![]() 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①在400℃时,2NH3(g)![]() N2(g)+3H2(g)的K′=________(填数值)。
N2(g)+3H2(g)的K′=________(填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正________v(N2)逆(填“>”、“<”、“=”或“不能确定”)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡________移动(填“向左”、“向左”或“不”);反应的ΔH__________(填“增大”、“减小”或“不改变”)。
(3)水煤气转化反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下两组教据:
CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下两组教据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
① 实验l中以CO2表示的反应速率为v(CO2)=____________;
② 实验1的平衡常数K1__________实验2的平衡常数K2(填“大于””小于,“等于”“不能确定”)。
③ 该反应正方向为_____________(填“吸”或‘放”)热反应;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京奥运会主体育场——“鸟巢”,被《泰晤士报》评为全球“最强悍”工程,“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料,有关说法正确的是
A.ETFE膜![]() 是由两种单体缩聚而成的
是由两种单体缩聚而成的
B.已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2
C.合金的熔点通常比组分金属高,硬度比组分金属小
D.用金属铝与V2O5冶炼钒,铝作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示:
异丁醇 | 叔丁醇 | |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用蒸馏的方法可将叔丁醇从二者的混合物中分离出来
D. 两种醇发生消去反应后得到同一种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下化学反应:![]() 现有容积相同且固定不变的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量
现有容积相同且固定不变的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量![]() 如表所列:
如表所列:
容器 |
|
| N2(mol) |
|
甲 | 2 | 1 | 0 |
|
乙 | 1 |
| 0 |
|
丙 | 1 |
| 1 |
|
根据以上数据,下列叙述不正确的是
A.![]()
B.![]()
C.![]()
D.在上述条件下反应生成![]() 气体放热
气体放热![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准盐酸滴定未知浓度的氢氧化钠溶液(酚酞作指示剂)用“偏高”“偏低”或“无影响”填空。
(1)酸式滴定管未用标准溶液润洗______
(2)锥形瓶用待测液润洗 ________
(3)锥形瓶洗净后还留有蒸馏水_______
(4)放出碱液的滴定管开始有气泡,放出碱液后气泡消失________
(5)酸式滴定管滴定前有气泡,滴定终点时气泡消失_________
(6)部分酸液滴出锥形瓶外________
(7)酸式滴定管滴定前读数正确,滴定后俯视读数_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com