
配制250mL0.10mol·L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
A. 转移溶液后未洗涤烧杯和玻璃棒就直接定容
B. 所用NaOH已经潮解
C. 带游码的天平称2.4gNaOH时误用了“左码右物”方法
D. 在容量瓶中进行定容时俯视刻度线
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期期中化学试卷(解析版) 题型:选择题
白磷与氧气可发生如下反应:P4+5O2 = P4O10。已知断裂下列化学键需要吸收的能量分别为:E(P—P) = a kJ·mol-1、E(P—O) = b kJ·mol-1、E(P=O) = c kJ·mol-1、E(O=O) = d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
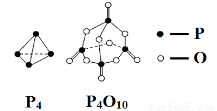
A.-(6a-12b-4c+5d)kJ·mol-1
B.-(-6a+12b+4c-5d)kJ·mol-1
C.-(-4a+6b+4c-5d)kJ·mol-1
D.-(4a-6b-4c+5d)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:
4Al(s)+3O2(g)=2Al2O3(s) ΔH1;
4Al(s)+2O3(g)=2Al2O3(s) ΔH2;
3O2(g)=2O3(g) ΔH3。则:
A.ΔH1-ΔH2=ΔH3 B.ΔH1+ΔH2=ΔH3
C.ΔH2-ΔH1=ΔH3 D.ΔH2+ΔH1+ΔH3=0
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:填空题
现有下列九种物质:①盐酸 ②石墨 ③蔗糖 ④CO2 ⑤熔融NaHSO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧硫酸 ⑨明矾
(1)属于电解质的有_________________________;
属于非电解质的有__________________________;
能导电的物质有____________________________。
(2)②和SiO2在高温下可发生如下反应:
3C+SiO2 SiC+2CO
SiC+2CO
上述反应中还原产物是 ;氧化剂与还原剂物质的量之比为  。
。
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-===H2O,该离子反应对应的化学方程式为________________________
(4)⑤的电离方程式为______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
已知:2Fe + 3Br2=2FeBr3,Fe2+的还原性大于Br-。现有16.8 g铁和0.3 mol Br2反应后加入水得到澄清溶液后,通入 a mol Cl2。下列叙述不正确的是
a mol Cl2。下列叙述不正确的是
A.当a=0.1时,发生的反应为2Fe2++Cl2=2Fe3++2Cl-
B.当a=0.45时,发生的反应为2Fe2++4Br-+3Cl 2=2Fe3++2Br2+6Cl-
2=2Fe3++2Br2+6Cl-
C.若溶液中Br-有一半被氧化时,c(Fe3+):c(Br-):c(Cl-)=1:1:3
D.当0<a<0.15时,溶液中始终满足2c(Fe2+)+3c(Fe3+)+c(H+)=c(C l-)+c(Br-)+c(OH-)
l-)+c(Br-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
在下列各组物质中,分子数一定相同的是 ( )
A.0.2mol H2和4.48L HCl气体
B.标准状况下1mol O2和22.4L H2O
C.4g 氦气和标准状况下22.4LCO2
D.4L CO和4L CO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:填空题
按要求写出反应方程式
①H++OH-=H2O(写出对应的化学方程式) 。
②CaCO3+2H+═Ca2++CO2↑+H2O(写出对应的化学方程式) 。
③向澄清石 灰水中通入过量CO2(写出对应离子方程式) 。
灰水中通入过量CO2(写出对应离子方程式) 。
④向NaHSO4溶液中滴入Ba(OH)2溶液至SO42-恰好完全沉淀(写出对应离子方程式) 。
(已知NaHSO4=Na++H++SO42-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省郏县一高、叶县二高等五校高二上期中化学卷(解析版) 题型:填空题
(1)反应mA+nB pC在某温度下达到平衡。
pC在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是___________.
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向___________方向移动.
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为___________态.
(2)乙二酸俗名草酸,易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
某学习小组的同学设计了如下实验方法测草酸晶体(H2C2O4·xH2O)中x值。
①称取1.260g纯草酸晶体,将其酸制成100.00mL水溶液为待测液
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00mL;
(1)滴定时,KMnO4标准液应装在 式滴定管中
(2)本实验滴定达到终点的标志是___________
(3)通过上述数据,计算出x=___________
讨论:若滴定终点时俯视滴定管刻度,则由此测得的x值会___________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上学期期中化学试卷(解析版) 题型:填空题
在0.2 L NaCl、MgCl2的混合溶液中,部分离子浓度大小如右图所示,回答下列问题:
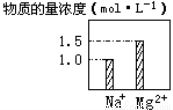
⑴该混合溶液中,Na+的物质的量为_________mol,MgCl2的物质的量为_________mol,Cl-的物质的量为_________mol。
⑵该混合溶液中含溶质的总质量为___________g 。
⑶将该混合溶液加水稀释至体积为 1 L,稀释后溶液中Cl-的物质的量浓度为_____mol·L-1 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com