
分析 (1)试管加热后温度很高;
(2)当试管内所盛液体超过容积的$\frac{1}{3}$时,加热后溶液容易溅出;
(3)烧瓶垫石棉网加热的目的是让烧瓶受热均匀;
(4)烧杯可用于加热液体试剂,不能用于灼烧;
(5)浓硫酸的沸点高于100℃.
解答 解:(1)试管加热后温度很高,故用手拿试管加热容易造成手被烫伤,故答案为:容易造成手被烫伤;
(2)当试管内所盛液体超过容积的$\frac{1}{3}$时,加热后溶液容易沸腾从而溅出伤人,故答案为:溶液沸腾溅出伤人;
(3)烧瓶垫石棉网加热的目的是让烧瓶受热均匀,否则容易炸裂,故答案为:烧瓶容易炸裂;
(4)烧杯可用于加热液体试剂,不能用于灼烧,如果用于固体试剂的干烧,容易造成烧杯的炸裂,故答案为:烧杯容易炸裂;
(5)浓硫酸的沸点高于100℃,故用量程为100℃的水银温度计测定浓硫酸的沸点,会造成温度计的炸裂,故答案为:会造成温度计的炸裂;
点评 本题考查了实验过程中的错误操作可造成的后果,难度不大,理解并记住错误操作的后果才能能理解正确的操作.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
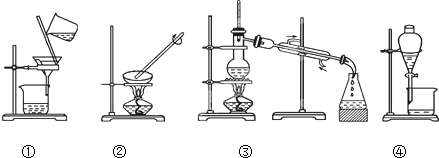
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
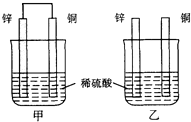
| A. | 两烧杯中铜片表面均有气泡产生 | B. | 甲中铜片是正极,锌片是负极 | ||
| C. | 两烧杯中溶液的pH均增大 | D. | 产生气泡的速度甲比乙快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③⑤ | C. | ①②③④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量钠保存在汽油中 | |
| B. | 固态碘盛放在细口玻璃瓶中 | |
| C. | 液溴保存在加有少量水的盖有玻璃塞的棕色细口瓶中 | |
| D. | 浓硝酸盛放在盖有橡胶塞的棕色瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al 和Mg | B. | K和 Na | C. | Na 和Al | D. | Zn 和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com