
【题目】(1)CH3COONa的水溶液呈_____(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):______________________; 溶液中含有各离子浓度从大到小的顺序为________________;
(2)氯化铝水溶液呈________性 ,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_________________________;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 ____________;
(3)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。常温时的pH _____7,该溶液中HSO3-的电离程度______HSO3-的水解程度。(填“>”、“=”、“<”)
【答案】 碱 CH3COO—+ H2O ![]() CH3COOH +OH- c(Na+)>c(CH3COO-)>c(OH-)>c(H+) 酸 Al3++3H2O
CH3COOH +OH- c(Na+)>c(CH3COO-)>c(OH-)>c(H+) 酸 Al3++3H2O ![]() Al(OH)3+3H+ Al2O3 小于 大于
Al(OH)3+3H+ Al2O3 小于 大于
【解析】(1)CH3COONa属于强碱弱酸盐,醋酸根离子水解,CH3COO—+ H2O ![]() CH3COOH +OH-,溶液呈碱性; 溶液中含有的离子浓度从大到小的顺序为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故答案为:碱;CH3COO—+ H2O
CH3COOH +OH-,溶液呈碱性; 溶液中含有的离子浓度从大到小的顺序为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故答案为:碱;CH3COO—+ H2O ![]() CH3COOH +OH-;c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
CH3COOH +OH-;c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
(2)AlCl3为强酸弱碱盐,Al3+水解:Al3++3H2OAl(OH)3+3H+,溶液呈酸性,氯化铝溶液蒸干,水解生成的氯化氢挥发,促进水解,蒸干得到的产物为氢氧化铝,灼烧得到氧化铝;
故答案为:酸;Al3++3H2OAl(OH)3+3H+;Al2O3;
(3)NaHSO3溶液中滴入石蕊,溶液变红,显酸性,pH<7,以电离为主,电离程度大于水解程度,故答案为:小于;大于。


科目:高中化学 来源: 题型:
【题目】工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g) ,为了寻找合适的温度,研究者进行了多次实验,每次实验保持原料气组成(3mol CO、3mol H2)、体积(10L)、反应时间等因素不变,实验结果如图所示。下列说法正确的是
CH3OCH3(g)+CO2(g) ,为了寻找合适的温度,研究者进行了多次实验,每次实验保持原料气组成(3mol CO、3mol H2)、体积(10L)、反应时间等因素不变,实验结果如图所示。下列说法正确的是

A.X、Y两点对应的CO正反应速率相等
B.合成二甲醚的正反应△H>0
C.反应温度控制在240℃~260℃之间
D.选择合适催化剂,可以提高CO的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚硝酰(NOCl)具有强氧化性,易与水反应生成HCl和氮氧化物。实验室可通过反应Cl2+2NO![]() 2NOCl △H<0制备
2NOCl △H<0制备
回答下列问题:
(1)甲组同学拟用下图所示装置(夹持仪器未画出)拟制备Cl2和NO。

①制取Cl2时,分液漏斗中加入浓盐酸,则烧瓶中放入的固体药品可能是______。
②制取NO时,铜与稀硝酸反应的离子方程式为_________。
(2)乙组的同学制氯化亚硝酰(沸点为-5.5℃)的装置如下:
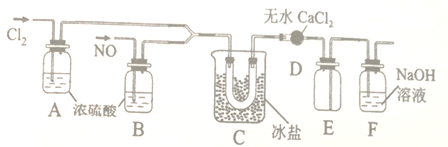
①装置D的作用是___________;装置E的作用是________。
②装置C中冰盐冷却的目的是___________(写两点)。
(3)丙组依据文献记载,氯化亚硝酰也可用NaNO2固体与气体制备,该反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制250mL0.5mol/L的NaOH溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥500mL容量瓶、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、⑩坩埚,需要用到的仪器有( )
A. ①③④⑥⑨⑩ B. ①④⑦⑧⑨⑩
C. ①③④⑦⑧⑨ D. ①②④⑤⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
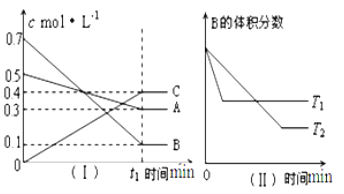
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为_________,达到平衡时A的转化率为_____。T1____T2(大于,小于,等于),正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有___________(填字母编号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,生成物的总能量小于反应物总能量的是
A. 碳在氧气中燃烧
B. 氢气还原氧化铜
C. Ba(OH)28H2O与NH4Cl(固体)的反应
D. 焦碳在高温下与水蒸气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)2C(g),反应曲线(T表示温度,P表示压强,C%表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )

A. 该反应是吸热反应
B. x=2
C. P3<P4,y轴可表示混合气体的相对分子质量
D. P3>P4,y轴可表示C物质在平衡体积中的百分含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出电离方程式
NaHCO3:______________;
H2SO4:________________;
KHSO4:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com