
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
科目:高中化学 来源:2014-2015广东省肇庆市高二上学期期末考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子能在指定环境中大量共存的是
A.pH=13的溶液:SO32-、Na+、AlO2-
B.使甲基橙溶液变红色的溶液:Na+、SO42-、HCO3-
C.在c(H+)=10-12mol/L的溶液:NH4+、Cl-、NO3-
D.加入足量Na2O2后的溶液:K+、Cl-、ClO-
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市五校高二上学期期末联考化学试卷(解析版) 题型:选择题
关于小苏打水溶液的表述正确的是
A.c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
B.c(Na+)+ c(H+) = c(HCO3-) + c(OH-) + c(CO32-)
C.HCO3-的电离程度大于HCO3-水解程度
D.存在的电离有NaHCO3 = Na+ + HCO3-、HCO3- CO32- + H+、H2O
CO32- + H+、H2O  H+ + OH-
H+ + OH-
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(14分)某工业原料主要成分是NH4Cl、FeCl3和AlCl3。利用此原料可以得到多种工业产品。分析下面流程,回答问题。

已知:Ksp[Fe(OH)3]=4.0×10-38
(1)用稀硫酸中和等体积等pH值的氨水和烧碱溶液,前者需要消耗的酸液体积 (填“大”“小”或“相同”)
(2)计算溶液②中Fe3+的物质的量浓度为 mol/L
(3)缓冲溶液中存在的平衡体系有: 、 、
此时溶液中c(NH4+) c(Cl-)(填>、=、<)。
(4)在缓冲溶液中加入少量盐酸或者NaOH溶液,溶液的pH值几乎依然为9.2。简述原理:
请举出另一种缓冲溶液的例子(写化学式) 。
(5)常温下向较浓的溶液④中不断通入HCl气体,可析出大量AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,电极Ⅰ为 Zn,电极Ⅱ为Cu,其他电极均为石墨,则下列说法正确的是
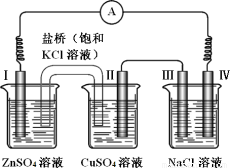
 A.电流方向:电极Ⅳ → ○ → 电极Ⅰ
A.电流方向:电极Ⅳ → ○ → 电极Ⅰ
B.盐桥中的K+会移向ZnSO4溶液
C.处得到标况下气体2.24L,电极II上析出6.4g固体
D.NaCl溶液中,电极Ⅲ制得氯气,电极Ⅳ制得金属钠
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列溶液一定呈中性的是
A.pH = 7的溶液
B.Kw = c(H+)·c(OH-) = 1.0×10-14的溶液
C.c(H+) = c(OH-)
D.pH = 3的酸与pH = 11的碱等体积混合后的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期期中考试化学试卷(解析版) 题型:填空题
(10分)臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是 和 (填分子式)。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。

①pH增大能加速O3分解,表明对O3分解起催化作用的是 。
②在30℃、pH=4.0条件下,O3的分解速率为 。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为 (填字母代号)。
A.40 ℃、pH=3.0 B.10 ℃、pH=4.0 C.30 ℃、pH=7.0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高一上学期期中考试化学卷(解析版) 题型:计算题
(7分)标准状况下,H2和CO的混合气体共8.96L,测得其质量为6.0g,试计算此混合气体中H2和CO的质量和体积各为多少?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省新密市高三第三次月考化学试卷(解析版) 题型:选择题
如下图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O
下列说法正确的是

A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com