
三聚氰酸![]() 可用于消除汽车尾气中的氮氧化物(如
可用于消除汽车尾气中的氮氧化物(如![]() )。当加热至一定温度时,它发生如下分解:
)。当加热至一定温度时,它发生如下分解:![]()
![]() (异氰酸,其结构是H-N=C=O)能和
(异氰酸,其结构是H-N=C=O)能和![]() 反应生成
反应生成![]() 、
、![]() 和
和![]() 。
。
(1)写出![]() 和
和![]() 反应的化学方程式。分别指明化合物中哪种元素被氧化?哪种元素被还原?标出电子转移的方向和数目。
反应的化学方程式。分别指明化合物中哪种元素被氧化?哪种元素被还原?标出电子转移的方向和数目。
(2)如按上述反应式进行反应,试计算吸收![]() 气体所消耗的三聚氰酸
气体所消耗的三聚氰酸
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
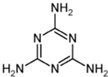 近期,质检部门在众多品牌乳制品中检出有毒有机物三聚氰胺[C3N3(NH2)3],其分子结构如图所示.在乳制品行业掀起了一场轩然大波,引发了一场关于食品安全问题的大讨论.三聚氰胺是一种重要的有机化工原料,因其含氮量高而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量指标,因此三聚氰胺也被人称为“蛋白精”.三聚氰胺遇强酸或强碱水溶液水解,氨基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3].三聚氰酸可用于消除汽车尾气中的NO2,其反应原理为:C3N3(OH)3=3HNCO;8HNCO+6NO2=7N2+8CO2+4H2O.下列说法正确的是( )
近期,质检部门在众多品牌乳制品中检出有毒有机物三聚氰胺[C3N3(NH2)3],其分子结构如图所示.在乳制品行业掀起了一场轩然大波,引发了一场关于食品安全问题的大讨论.三聚氰胺是一种重要的有机化工原料,因其含氮量高而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量指标,因此三聚氰胺也被人称为“蛋白精”.三聚氰胺遇强酸或强碱水溶液水解,氨基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3].三聚氰酸可用于消除汽车尾气中的NO2,其反应原理为:C3N3(OH)3=3HNCO;8HNCO+6NO2=7N2+8CO2+4H2O.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、C3N3(OH)3与HNCO为同一物质 |
| B、HNCO是一种很强的氧化剂 |
| C、1mol NO2在反应中转移的电子为4mol |
| D、反应中NO2是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
三聚氰胺[C3N3(NH2)3]是一种重要的有机化工原料。动物长期摄入三聚氰胺会造成生殖、泌尿系统的损害,膀胱、肾部结石,并可进一步诱发膀胱癌,它遇强酸或强碱水溶液会水解,胺基逐步被羟基取代,最后生成三聚氰酸[C3N3(OH)3]。三聚氰酸可用于消除汽车尾气中的NO2,其反应原理为:C3N3(OH)3===3HNCO;8HNCO+6NO2==7N2+8CO2+4H2O,下列说法正确的是( )
A.C3N3(OH)3与HNCO为同一种物质
B.HNCO是一种很强的氧化剂
C.1 mol NO2在反应中得到的电子为4 mol
D.反应中CO2是氧化产物
查看答案和解析>>
科目:高中化学 来源:2012届江苏省高二学业水平测试模拟演练化学试卷 题型:选择题
国家质检总局调查结果显示:所谓毒奶粉是被三聚氰胺所污染,它可由三聚氰酸[C3N3(OH)3]制备.三聚氰酸可用于消除汽车尾气中的NO2,已知三聚氰酸中氮元素的化合价为-3价,HCNO中N为-3价,O为-2价,有关反应原理为:
①
C3N3(OH)3 3HCNO;
②
8HCNO+6NO2
3HCNO;
②
8HCNO+6NO2 7N2+8CO2+4H2O
7N2+8CO2+4H2O
下列说法正确的是
A.反应①中的两种物质互为同素异形体 B.反应②中HCNO是氧化剂
C.反应②中NO2是还原剂 D.反应②中转移的电子数为24
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com