
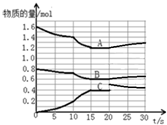
 在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )
在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )| A. | 反应在前10s 内v(B)=0.005mol/(L.s) | |
| B. | 方程式计量数a:b:c为2:1:2 | |
| C. | 10 s时改变条件可能是升高温度,20s时平衡逆向进行 | |
| D. | 15~20s间,反应的平衡常数是2.7 |
分析 A、反应在前10s内,根据v(B)=$\frac{△c}{△t}$来计算;
B、方程式计量数之比等于各物质浓度(物质的量)变化量之比;
C、升高温度,反应正向进行,速率加快,根据影响平衡移动的因素来回答;
D、根据反应的平衡常数K=$\frac{产物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$来计算.
解答 解:A、反应在前10s内,根据v(B)=$\frac{△c}{△t}$=$\frac{\frac{0.8mol-0.7mol}{2L}}{10s}$=0.005mol/(L.s),故A正确;
B、方程式计量数之比等于各物质浓度(物质的量)变化量之比,方程式计量数a:b:c=(1.6-1.4):(0.8-0.7):(0.2-0)=2:1:2,故B正确;
C、升高温度,反应正向进行,速率加快,20s时,反应物的量逐渐增加,产物的量减少,所以平衡逆向进行,故C正确;
D、反应的平衡常数K=$\frac{产物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$=$\frac{0.{2}^{2}}{0.{6}^{2}×0.3}$=0.37,故D错误.
故选D.
点评 本题考查了化学反应速率影响因素,化学反应速率、化学平衡常数的计算,图象分析和化学平衡移动原理是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 稀醋酸中加入少量冰醋酸能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的盐酸与氨水混合后,溶液pH=7 | |
| C. | 0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) | |
| D. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若误饮c(Ba2+)=1.0×10-5mol/L溶液时,不会引起Ba2+中毒 | |
| B. | 因为Ksp(BaCO3)>Ksp(BaSO4),所以BaCO3不能作内服造影剂 | |
| C. | 向同浓度Na2SO4和Na2CO3的混合溶液中滴加BaCl2溶液,BaSO4先析出 | |
| D. | 在BaSO4和BaCO3共存的悬浊液中,c(SO42-):c(CO32-)=1:51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和热测定 | B. | 中和滴定 | ||
| C. | 过滤 | D. | 物质的量浓度溶液配制 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水中有下列平衡Cl2+H2O═HCl+HClO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 氨水中加入NaOH固体有利于氨气的溢出 | |
| D. | pH=1的盐酸加水稀释到原体积的100倍后,PH=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10.5% | B. | 9.1% | C. | 8% | D. | 5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S与Cu反应:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| B. | 酸雨放置过程中pH变小:2H2SO3+O2═2H2SO4 | |
| C. | 亚硫酸氢钙溶液与澄清的石灰水混合:Ca2++HSO3-+OH-═CaSO3↓+H2O | |
| D. | 向Na2S和Na2SO3的混合溶液中滴加稀H2SO4[n(Na2S):n(Na2SO3)=2:1]:2S2-+SO32-+6H+═3S↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去N2中的O2:通过灼热的CuO粉末,收集气体 | |
| B. | 某吸热反应能自发进行,则该反应一定是熵增的反应 | |
| C. |  如图是从化学试剂商店买回的硫酸试剂标签,配制80mL2.3mol•L-1的稀硫酸需量取该硫酸12.5 mL | |
| D. | 下列各种物质在一定条件下反应,所得产物与反应物的用量或与反应条件无关①Na2SiO3+CO2+H2O ②Fe+Cl2 ③Ca(HCO3)2+Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com