
(8分)已知:①MnO4—
+e- MnO42―
(绿色)(强碱性条件)
MnO42―
(绿色)(强碱性条件)
②MnO4—+ 8H+ + 5e- Mn2+ (无色)+ 4H2O(强酸性条件)
Mn2+ (无色)+ 4H2O(强酸性条件)
(1)在KOH溶液中,KMnO4与K2SO3溶液发生反应, 写出反应的离子方程式 。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式 .
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,MnO4‑ 具有氧化性,最合适的亚铁盐是 (选填编号),可用来酸化KMnO4溶液的试剂是 (选填编号)
a. FeCl2 b. FeSO4 c.Fe(NO3)2 d稀硫酸 e. 盐酸 f. 硝酸
(4)向20 mL浓度为0.05mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4‑ 全部转化为Mn2+ ,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于 mL
(共8分)(1) 2MnO4—+SO32―+ 2OH—=== 2MnO42―+SO42―+ H2O(2分)
(2) 4MnO4—+4OH—=== MnO42―+2H2O +O2↑(2分)
(3) b d(各1分,共2分)(4)8ml(2分)
【解析】由题目所给条件可知MnO4— 在酸性、碱性条件下氧化能力不同:在强碱性条件下生成MnO42―、在酸性条件下生成Mn2+。
(1)(2)一般是根据化合价的升降守恒、电荷守恒、原子守恒进行离子方程式的配平
(3)由于氯离子可还原MnO4—、NO3—在酸性条件下氧化性很强,故最合适的亚铁盐是FeSO4,酸化KMnO4溶液的试剂最好是硫酸
(4)由方程式MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O可得所需c(H+)=1mol/L的硫酸体积为:
V=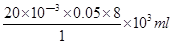 =8
ml
=8
ml


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| 加入药品 | 不加MnSO4的硫酸 酸化的H2C2O4溶液 |
加少量MnSO4的硫酸 酸化的H2C2O4溶液 |
| 实验现象 (褪色时间)/s |
H2C2O4褪色很慢 (31秒) |
H2C2O4褪色很快(4秒) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管A | 试管B | |
| 加入试剂 | ||
| (预期)实验现象 (褪色时间) |
||
| 结论 | 猜想Ⅱ正确 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾( FeSO4·7H2O)。
⑴若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1: ▲ 。
⑵为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为 ▲ 。
⑶硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V mL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+——Mn2++Fe3++H2O(未配平)
①V的取值范围为 ▲ ;
②若V=35,试计算混合物中CuS的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com