
分析 (1)水的电离是吸热的过程,水的离子积常数随温度的升高而增大;
(2)纯水中,水电离出的氢离子和氢氧根离子浓度是相等的;
(3)根据95℃时水的离子积Kw=1×10-12,而在碱溶液中,氢氧根几乎全部来自于碱的电离,根据水的离子积来计算.
解答 解:(1)因为此温度下的KW=1.0×10-12大于25℃时的KW=1.0×10-14,说明此温度高于25℃,故答案为:>;
(2)只要是纯水中,不管温度高低,水电离出的氢离子和氢氧根离子浓度是相等的,即95℃纯水中c(H+)=c(OH-),故答案为:=;
(3)根据95℃时水的离子积Kw=1×10-12,而在碱溶液中,氢氧根几乎全部来自于碱的电离,即溶液中的c(OH-)=1×10-1mol/L,根据水的离子积可知,溶液中的C(H+)=$\frac{1{0}^{-12}}{0.1}$=10-11mol/L,故pH=-lgC(H+)=11,故答案为:11.
点评 本题考查学生水的电离平衡移动的因素和溶液pH的计算等方面的知识,注意知识的归纳和整理是解题关键,难度不大.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:填空题
 可简写为
可简写为  .降冰片烯的分子结构可表示为
.降冰片烯的分子结构可表示为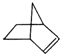
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+=Fe2++Cu | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与盐酸反应:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com