
(4分)利用氧化还原反应原理配平
⑴ NH3
+ O2 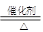 NO + H2O
NO + H2O
⑵ FeSO4 + KNO3 + H2SO4 = K2SO4 + Fe2(SO4)3 + NO↑+ H2O
 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
| A、胶体的分散质粒子直径大小介于溶液与浊液之间 | B、金属冶炼通常利用氧化还原反应原理 | C、陶瓷、水泥和光导纤维均属于硅酸盐材料 | D、“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霆天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)(1)(3分)下列各组物质中: ③H2O和 D2O ④ CH3CH3 和CH3CH2CH2CH3 ⑤ CH3-CH2-OH和CH3-O-CH3
互为同位素的是;____ __; 互为同素异形体是:____ __;
互为同分异构体是:___ ___。
(2)(5分)利用氧化还原反应原理配平以下化学方程式,并填空:
FeSO4 + KNO3+ H2SO4=== K2SO4+ Fe2(SO4)3+ NO↑+ H2O
①氧化产物为
②当电子转移了0.3mol时,有 g氧化剂参加反应
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.0.1molNa2O2中含有的离子数为0.4NA
B.利用氧化还原反应原理制取1mol氧气,转移的电子数一定为4NA
C.7.1g氯气与足量NaOH溶液反应电子转移数为0.2NA
D.标准状况下,和
混合气体中含有的原子数是
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省高三上学期11月月考化学试卷 题型:选择题
若NA表示阿伏加德罗常数的值,下列说法正确的是
|
A.0.1molNa2O2中含有的离子数为0.4NA |
|
B.利用氧化还原反应原理制取1mol氧气,转移的电子数一定为4NA |
|
C.7.1g氯气与足量NaOH溶液反应电子转移数为0.2NA |
|
D.0.1mol氯气与金属铁完全反应时,转移电子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com