
【题目】Cr2O72-和CN-是工业废水中常见的污染物。若利用下列流程可对分别含两种离子的废水进行综合处理:

回答下列问题:
(1)已知步骤②中无气体生成,写出反应的离子方程式_______________,步骤④中NaClO可将CNO-处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,写出这两种气体的化学式___________________。
(2)步骤⑥的反应为 S2O32-+ Cr2O72-+2H+→SO42-+ Cr3++H2O(未配平),则每处理1mol Cr2O72-离子转移_______mol电子。
(3)步骤⑦的操作名称为_______,该操作所需的玻璃仪器为____________。
(4)CrO42-和Cr2O72-在溶液中可相互转化,用离子方程式表示K2Cr2O7溶液中的转化反应_____。
(5)Cr3+也有一定毒性,会污染水体,常温下要除去废液中多余的Cr3+,调节pH至少为_______,才能使铬离子沉淀完全(铬离子浓度应小于10-5mol/L)。已知Cr(OH)3的溶度积为6.3×10-31, ![]() ≈4,lg2≈0.3。
≈4,lg2≈0.3。
【答案】 CN-+ClO-=CNO-+Cl- N2、CO2 6 过滤 漏斗、玻璃棒、烧杯 Cr2O72-+H2O![]() 2CrO42-+2H+ 5.6
2CrO42-+2H+ 5.6
【解析】含CN-废水调整溶液PH加入NaClO溶液,步骤②中无气体生成,氧化CN-离子反应生成CNO-的废水,步骤④中NaClO可将CNO-处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,生成气体为N2、CO2,溶液A含有NaCl、NaOH等溶质,含Cr2O72-的废水调整溶液PH加入Na2S2O3发生氧化还原反应得到含硫酸根离子的废水,Cr2O72-被还原生成Cr3+,和含CNO-的废水继续处理得到滤渣C为Cr(OH)3,滤液D主要含有硫酸钠;
(1)步骤②中无气体生成,NaClO氧化CN-离子反应生成CNO-的废水,反应的离子方程式为CN-+ClO-═CNO-+Cl-,步骤④中NaClO可将CNO-处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,由物质的组成元素可知应为N2、CO2;
(2)反应S2O32-+Cr2O72-+H+-→SO42-+Cr3++H2O中,Cr元素化合价有+6价降低到+3价,则每处理1molCr2O72-转移6mol电子;
(3)步骤⑦用于分离固体和液体,应为过滤操作,用到的玻璃仪器有漏斗、玻璃棒、烧杯;
(4)用离子方程式表示K2Cr2O7溶液中的转化反应为Cr2O72-+H2O![]() 2CrO42-+2H+;
2CrO42-+2H+;
(5)除去废水中的Cr2+,可先通入氧气或空气,将Cr2+氧化为Cr3+,然后加入碱液调节溶液的pH,要使铬的离子沉淀完全,c(Cr3+)<10-5mol/L,则c(OH-)=![]() mol/L=4×10-9mol/L,pH=-lg(
mol/L=4×10-9mol/L,pH=-lg(![]() )=5.6。
)=5.6。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】化学在人类生活中扮演着重要角色,下列应用不正确的是( )
A.明矾可用于水的杀菌,消毒
B.盐卤可用于制豆腐
C.目前加碘食盐主要添加的是KIO3
D.在空气质量日报中SO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学电池的说法中正确的是
A.化学电池只能将化学能转化为电能
B.燃料电池能将全部化学能转化为电能
C.锌银电池比能量大,电压稳定,储存时间长
D.一次电池包括干电池和蓄电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H为芳香酯,其合成路线如下:
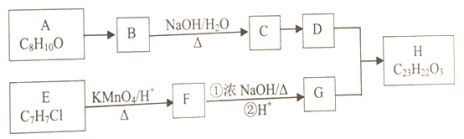
已知以下信息:
①A—H均为芳香族化合物,A的苯环上只有一个取代基,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。
② 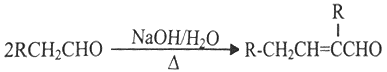
③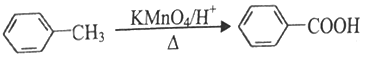
请回答下列问题:
(1)A→B的反应类型为____________,G所含官能团的名称为 ________________。
(2)B与银氨溶液反应的化学方程式为_____________________。
(3)H的结构简式为____________。
(4)符合下列要求的A的同分异构体有________________种。
①遇氯化铁溶液显紫色 ②属于芳香族化合物
其中苯环上有两个取代基的有 ___________________ (写结构简式)
(5)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)______________合成路线流程图示例如下:
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2NO2 ![]() 2NO + O2在体积不变的密闭容器中反应,现有以下几种说法:
2NO + O2在体积不变的密闭容器中反应,现有以下几种说法:
①反应混合物中各物质的物质的量浓度相等
②单位时间内生成n mol O2 的同时生成2n mol NO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均摩尔质量不再改变的状态
其中表示达到平衡状态的表述是( )
A.①④ B.②④⑥ C.①②③ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应:N2+3H3![]() 2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
2NH3是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
⑴相同条件下,1 mol N2和3 mol H2所具有的能量________(“大于”、“小于”、“等于”)2 molNH3具有的能量;
⑵如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量_______(“大于”、“小于”、“等于”)上述数值,其原因是_____________;
⑶实验室模拟工业合成氨时,在容器为2L的密闭容器内,反应经过10min后,生成10 mol NH3,则用N2表示的该反应速率为:_____________;
⑷一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是_______
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值 d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等 f.反应达到最大限度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于ΔH-TΔS的说法中正确的是
A.ΔH-TΔS可用于判断所有条件下的反应能否自发进行
B.ΔH-TΔS只用于判断温度、体积一定的反应能否自发进行
C.ΔH-TΔS只用于判断温度、压强一定的反应能否自发进行
D.某反应ΔH-TΔS<0,则该条件下此反应一定剧烈进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。

(1)该物质的结构简式为___________________。
(2)该物质中所含官能团的名称为_____________________。
(3)下列物质中,与该产品互为同系物的是__________________,与该产品互为同分异构体的是__________________。(填序号)
①CH3CH="==CHCOOH"
②CH2===CHCOOCH3
③CH3CH2CH===CHCOOH
④CH3CH(CH3)COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素。X与W可形成四面体形的共价化合物,该化合物常用作灭火剂。Y的次外层电子数等于其最外层和最内层电子数之和的2倍,Y、Z的最外层电子数之和等于W的最外层电子数。
(1)用化学符号表示X的一种核素 。
(2)写出Y的单质与X的最高价氧化物反应的化学方程式 。
(3)Z的单质在W的单质中燃烧,生成的产物中各原子的最外层均达到8电子稳定结构的分子为 。
(4)用电子式表示Y与W形成化合物的过程为 。
(5)XW4的电子式为 。
(6)W的氢化物R是实验室一种常用试剂的主要成分,该试剂可用于实验室多种气体的制备,写出实验室制取气体时满足下列条件的离子方程式。
①R作氧化剂: 。
②R作还原剂: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com