
【题目】下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请填写下列空白。
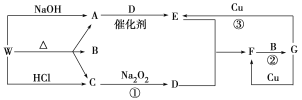
(1)化合物W可能是________或__________(填化学式),C的结构式是________,
(2)D的组成元素在周期表中的位置是__________。
(3)反应③的离子方程式:________________________。
(4)已知在催化剂作用下,E与CO反应生成参与大气生态循环的无毒物质,请写出该反应的化学方程式 。
(5)在反应②中,发生还原反应和氧化反应的物质的质量之比为__________。
【答案】
(1)(NH4)2CO3或NH4HCO3;O=C=O
(2)第二周期第ⅥA族
(3)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
(4)2NO+CO![]() N2+CO2
N2+CO2
(5)1:2
【解析】
试题分析:W能和NaOH、HCl反应生成无色气体,A和D反应生成E,C能和过氧化钠反应生成D,且W能分解生成两种气体,D能和E反应生成F,F和B反应生成G,E、F中含有相同元素,G能和Cu反应生成两种物质,则G为HNO3,F为E为NO、D为O2、F为NO2,W应该为铵盐,A为NH3、C为CO2,则B为H2O,W为(NH4)2CO3或NH4HCO3。
(1)通过以上分析知,W为(NH4)2CO3或NH4HCO3,C是二氧化碳,其结构式为O=C=O。
故答案为:(NH4)2CO3或NH4HCO3;O=C=O;
(2)D是氧气,O元素在周期表中位于第二周期第VIA族。
故答案为:第二周期第ⅥA族;
(3)该反应为Cu和稀硝酸反应生成NO,离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O。
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
(4)在催化剂作用下,NO与CO反应生成参与大气生态循环的无毒物质氮气和二氧化碳,反应方程式为2NO+CO![]() N2+CO2。
N2+CO2。
故答案为:2NO+CO![]() N2+CO2;
N2+CO2;
(5)该反应为3NO2+H2O=2HNO3+NO,该反应中有![]() 的二氧化氮作还原剂、有
的二氧化氮作还原剂、有![]() 的二氧化氮作氧化剂,所以发生还原反应和氧化反应的物质的质量之比为1:2。
的二氧化氮作氧化剂,所以发生还原反应和氧化反应的物质的质量之比为1:2。
故答案为:1:2。


科目:高中化学 来源: 题型:
【题目】下中的实验装置可用于制取乙炔。 请填空:
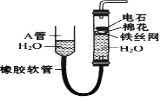
(1) 图中,A管的作用是_______________;制取乙炔的化学方程式是 。
(2)乙炔通入溴的CCl4溶液中观察到的现象是____________ ;乙炔发生了________反应。
(3)写出由乙炔制取聚氯乙烯的化学方程 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格。
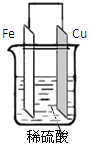
(1)正极是 (填“铜极”或“铁极”),现象是: ,电极反应是: ,发生 反应(填“氧化”或“还原”)。
(2)电流从 经导线流到 (填“铜极”或“铁极”)。
(3)若反应生成的氢气在标况下为4.48L,则反应过程中有 mol电子发生转移,溶解的铁质量为_____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为____________________________;
(2)A中的碳原子是否都处于同一平面?_________(填“是”或者 “否”);
(3)A是否存在顺反异构体?_________(填“是”或者“否”)。
(4)用系统命名法命名A为______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
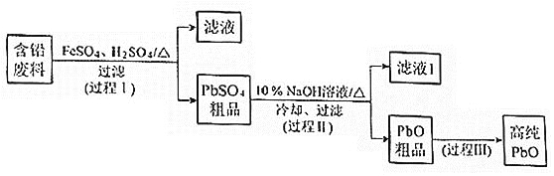
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42=2Fe3++PbSO4+2H2O
ii: ……
①写出ii的离子方程式:________________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.______________。
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq),其溶解度曲线如图所示。
NaHPbO2(aq),其溶解度曲线如图所示。
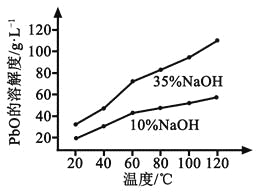
①过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是____._(选填序号)。
A.减少PbO的损失,提高产品的产率
B.重复利用氢氧化钠,提高原料的利用率
C.增加Na2SO4浓度,提高脱硫效率
②过滤Ⅲ的目的是提纯,综合上述溶解度曲线,简述过程Ⅲ的操作_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6 H2O===CaO2·8H2O
反应时通常加入过量的Ca(OH)2,其目的是_____________。
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有____________(填序号)。
A.Ca2+ B.H+ C.CO32– D.OH
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
![]()
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L1表示),写出计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有资料认为NO、NO2不能与Na2O2反应。某小组学生提出质疑,从理论上分析Na2O2和NO2都有氧化性,根据化合价升降原则提出假设并进行探究:
假设Ⅰ.Na2O2能氧化NO2
假设Ⅱ.NO2能氧化Na2O2
(1)小组甲同学设计了如图实验装置,并进行如下实验:
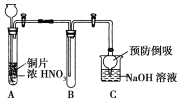
①试管A中发生反应的化学方程式是______________________________。
②待试管B中收集满气体,向试管B中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带余烬的木条迅速伸进试管内,看见木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,在A、B之间增加一个装置,该装置的作用是______________________________。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;但带余烬的木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的化学方程式是
_____________________________________________________________________。
(2)丙同学认为NO易被O2氧化,更易被Na2O2氧化。
查阅资料:①2NO+Na2O2===2NaNO2
②6NaNO2+3H2SO4===3Na2SO4+2HNO3+4NO↑+2H2O
③酸性条件下,NO或NO都能与MnO反应生成NO和Mn2+
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
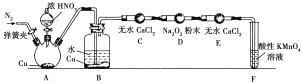
①A装置中盛装Cu片的仪器名称是__________,B中观察到的主要现象是______________________,F装置的作用是______________________________。
②在反应前,打开弹簧夹,通入一段时间N2,目的是______________________________。
③充分反应后,检验D装置中产物是NaNO2还是NaNO3的实验方法是____________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com