
| A�� | �������Һ�е����������ƶ� | |
| B�� | �ŵ�һ��ʱ���KOH�����ʵ���Ũ�Ȳ��� | |
| C�� | ͨ����ĵ缫Ϊ���� | |
| D�� | �μӷ�Ӧ��O2��C2H6�����ʵ���֮��Ϊ2��7 |
���� A�����Ӳ������������Һ��
B�����ݵ���ܷ�Ӧ�жϣ�
C��ȼ�ϵ����ȼ���ڸ�����Ӧ��
D�����ݵ�ʧ�������ȷ����������ȼ�ϵ����ʵ���֮�ȣ�
��� �⣺A���ŵ�ʱ���������Һ���������������ƶ������������ƶ������Ӳ������������Һ����A����
B����ط�ӦʽΪC2H6+4OH-+$\frac{7}{2}$O2=2CO32-+5H2O��KOH�����ʵ������١���Һ�����������KOH�����ʵ���Ũ�ȼ�С����B����
C��ȼ�ϵ���ڣ�ȼ��ʧ���ӷ���������Ӧ���������õ��ӷ�����ԭ��Ӧ������ͨ������ĵ缫�Ǹ�������C��ȷ��
D����ط�ӦʽΪC2H6+4OH-+$\frac{7}{2}$O2=2CO32-+5H2O����μӷ�Ӧ��������C2H6�����ʵ���֮��Ϊ7��2����D����
��ѡC��
���� ���⿼���˻�ѧ��Դ���͵�أ����ݵ�ʧ����ȷ����������Ӧ���ٽ�ϵ缫��Ӧʽ�������ƶ�������������������ƶ�������ж�Ϊ�״��㣮


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 | NaCl | K2SO4 | Na2SO4 |
| �� | 0.3mol | 0.2mol | 0.1mol |
| �� | 0.1mol | 0.3mol | 0.2mol |
| A�� | K+�����ʵ�����ͬ | B�� | Cl-�����ʵ�����ͬ | ||
| C�� | Na+�����ʵ�����ͬ | D�� | SO42-�����ʵ�����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ȶ��ԣ�H2S��HF | B�� | HCl�ĵ���ʽΪ | ||
| C�� | H2O��Ħ������Ϊ18 | D�� | ��±������HI���ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na | B�� | Fe | C�� | O | D�� | Ar |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��=�ڣ��ۣ��ܣ��ݣ��� | B�� | �ܣ��ۣ���=�ݣ���=�� | C�� | ��=�ޣ��ڣ��ۣ��ܣ��� | D�� | �ܣ��ۣ��ڣ��ݣ��٣��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 Lˮ���ܽ�1 mol NaCl���γ���Һ�����ʵ���Ũ��Ϊ1 mol•L-1 | |
| B�� | ��״���£�22.4 L HCl����1 Lˮ���γɵ���Һ���Ϊ1 L | |
| C�� | ��״���£���33.6 L HCl����ˮ�γ�1 L��Һ�������ʵ���Ũ����1.5 mol•L-1 | |
| D�� | 1 mol CaCl2����ˮ�γ�1 L��Һ��������Һ��c��Cl-������1 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ�м���С�մ���Һ�������ɫ��������ɫ���� | |
| B�� | ������˥�ߵȼ��������ѪҺ�ж���������ѪҺ���������� | |
| C�� | ˮ�೧��ұ���ø�ѹ��������̳����Լ��ٶԿ�������Ⱦ | |
| D�� | ţ�����ռ���Һ���ȣ���Ӧ������Һ�м���ʳ�Σ����й������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 $\stackrel{����}{��}$
$\stackrel{����}{��}$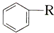 +HCl
+HCl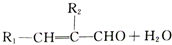
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com