
| A、密度较小 | B、易导电 |
| C、易导热 | D、银白色 |
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
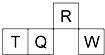 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、含T的盐溶液一定显酸性 |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、最简单气态氢化物的热稳定性:R>Q |
查看答案和解析>>
科目:高中化学 来源: 题型:
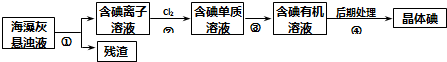
| A、步骤④的操作是过滤 |
| B、可用淀粉溶液检验步骤②的反应是否进行完全 |
| C、步骤①、③的操作分别是过滤、萃取 |
| D、步骤③中加入的有机溶剂可能是苯或CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
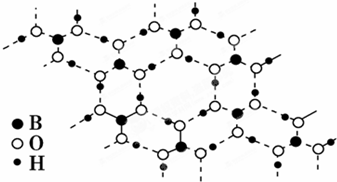
| A、正硼酸晶体属于原子晶体 |
| B、H3BO3分子的稳定性与氢键有关 |
| C、1 mol H3BO3晶体中含有3 mol氢键 |
| D、分子中硼原子最外层为8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10mL量筒量取5.20mL盐酸 |
| B、用托盘天平称取25.20g氯化钠 |
| C、用广泛pH试纸测得溶液的pH为4.2 |
| D、用25.00mL碱式滴定管量取14.80mL NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||
| B、在碳酸氢钠溶液中加入过量的氢氧化钡溶液:Ba2++OH-+HCO3-═BaCO3↓+H2O | ||
C、用新制的氢氧化铜悬浊液检验乙醛中的醛基:CH3CHO+2Cu(OH)2+OH-
| ||
| D、向Ca(ClO)2溶液中通入过量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+2H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com