
【题目】有a、b、c、d 四瓶无色溶液,它们分别是Ba(OH)2溶液,NaHCO3溶液、MgCl2溶液、稀硫酸中的某一种。现各取少量溶液进行两两混合,实验现象如下表所示,表中“↓”表示生成沉淀;“↑”表示生成气体;“一”表示无明显现象。下列推理不正确的是

A. c一定是稀硫酸 B. d一定是MgCl2溶液
C. a可能是NaHCO3溶液 D. b一定是Ba(OH)2溶液。
科目:高中化学 来源: 题型:
【题目】已知铜的配合物A(结构如图)。请回答下列问题:
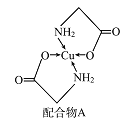
(1)Cu的简化电子排布式为______________ 。
(2)A所含三种元素C、N、O的第一电离能由大到小的顺序为_______________。其中氮原子的杂化轨道类型为________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比
是__________;N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,则N2O的电子式为_______。
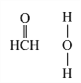
(4)在Cu催化下,甲醇可被氧化为甲醛(HCHO),甲醛分子中H CO的键角___________(选填“大于”、“等于”或“小于”)120°;甲醛能与水形成氢键,请在右图中表示出来___________。
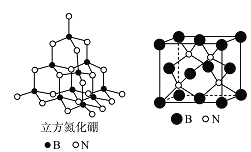
(5)立方氮化硼(如图)与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为___________;结构化学上用原子坐标参数表示晶胞内部各原子的相对位置,上图(右)立方氮化硼的晶胞中,B原子的坐标参数分别有:
![]() 等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。
等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理应用和处理元素化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
②尿素在一定条件下可将氮的氧化物还原为氮气。

根据图像,结合①中信息,尿素还原NO(g)的热化学方程式是_________。
③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:
CO2(g)+2NH3(g)![]() CO(NH2)2+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_____b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是_______。
CO(NH2)2+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_____b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是_______。
(2)在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应: 2CO(g)+SO2(g) ![]() S(g)+2CO2(g) △>0, 测得相关数据如下表所示。
S(g)+2CO2(g) △>0, 测得相关数据如下表所示。

下列说法不正确的是________
A.反应开始时的速率:丙>乙 B. b=1.6 C.平衡常数:甲>乙
(3)ClO2是一种安全稳定的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备ClO2原理如下:

①a电极上产生的NCl3分子,常温下是一种黄色粘稠的油状液体,该分子的电子式为______。
②电解池中总反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的说法不正确的是
A. 高纯硅具有良好的半导体性能,可制成硅芯片、光电池、光导纤维等
B. 二氧化硅能与氢氟酸反应,可用氢氟酸刻蚀玻璃
C. 向硅酸钠溶液中滴加稀盐酸有不溶物生成,实验室可用该方法制备硅酸
D. “硅胶”由硅酸凝胶经干燥、脱水制得,常用作食品、药品等的干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分〕某化学兴趣小组欲探究含硫物质的性质及制备。
【探究一】用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
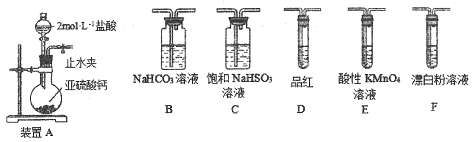
装置连接顺序为_________(用字母表示),其中装置C的作用是___________。
【探究二】
(1)某小组同学为探究SO2的漂白性性质,用下图所示装置进行实验,
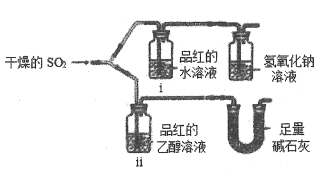
观察到如下现象:i中红色褪去;ii中无变化.碱石灰的作用除了吸收尾气外还有_______的作用。从实验中可知使品红的水溶液褪色的微粒可能是____________。
(2)该小组同学又对SO2与氯水的反应进行探究。
①用注射器吸入一定量的饱和氯水和SO2,振荡,静置,再吸入少量品红溶液,发现品红溶液不褪色。②改变氯水用量,重复①操作,发现品红溶液红色褪去,你认为②中品红溶液褪色的原因可能是__________。 设计一个实验(说明操作方法、现象及结论)来验证你的假设________。
【探究三】连二亚硫酸钠(Na2S2O4)俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。制取保险粉通常需要二氧化硫。
(1)制取Na2S2O4常用甲酸钠法。控制温度70-80℃,在甲醇溶液(溶剂)中溶解甲酸钠(HCOONa),再滴加Na2CO3溶液同时通SO2维持溶液酸性,即可生成Na2S2O4,反应的离子方捏式________。
(2)测定保险粉纯度。Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4酸性溶液发生反应:5Na2S2O4+6KMnO4+4H2SO4=5Na2SO4+3K2SO4+6MnSO4+4H2O。称取5.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL该溶液于锥形瓶中,用0.10mol·L-1的KMnO4溶液滴定。重复上述操作2次,平均消耗KMnO4溶液21.00mL.则该样品中Na2S2O4的质量分数为______ (杂质不参与反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①正常雨水的pH为7.0,酸雨的pH小于7.0;
②严格执行机动车尾气排放标准有利于防止大气污染;
③Fe2O3常用作红色油漆和涂料;
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害;
⑤SiO2可用于制太阳能电池。
A. ①②③ B. ①④⑤
C. ②③④ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究溶液导电性与离子浓度的关系,某课题小组设计了如下实验:
取一定质量Ba(OH)2溶液做导电性实验,往烧杯中滴加稀硫酸、装置如图1.测得溶液导电强度如图2所示。
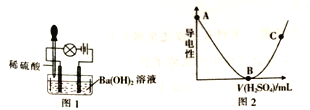
(1)根据组成分类、将盐分为正盐(如Na2CO3)、酸式盐(如NaHCO3)、碱式盐[如碱式碳酸铜Cu2(OH)2CO3等]。NaHSO4属于___________(填字母)。
A.钠盐 B.含氧酸 C.酸式盐 D.氧化物
(2)往烧杯中滴加稀硫酸的过程中,观察到灯泡变化:亮→暗→熄→亮,还可观察到的现象有_________。
(3)图2中,AB段变化的原因是__________;BC段变化的原因是_________。
(4)写出A→B过程中发生反应的离子方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是____________。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

① 一段脱水后,残留固体质量占原样品质量的64.5%,试确定生成物的化学式__________。② 二段脱水时,溶入H2和Cl2燃烧产物的目的是__________。
③ 该工艺中可循环使用的物质有_____________
(3)储氢材料Mg(AlH4)2在110-200℃的反应为:Mg(AlH4)2 =MgH2 +2Al+3H2↑,每转移6mol电子生成氢气的物质的量为__________mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。
① 40℃时,复盐开始热解生成MgCO3·3H2O,并有气体产生,该反应的化学方程式为________。
② 制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL 的溶液。
a.准确量取25.00mL 待测液,用0.1000 mol/ L AgNO3 标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为______________mL。

b.
AgCl | AgBr | AgI | Ag2CrO4 | |
Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
颜色 | 白 | 淡黄 | 黄 | 砖红 |
参照上表数据及信息分析,滴定时可以作指示剂的是________(填数字序号)。
① CaCl2 ② NaBr ③ NaI ④ K2CrO4
c.滴定时,应将溶液调成中性,不能是强酸性或强碱性,其中不能是强碱性的原因是________。
d.产品中氯的质量分数为___________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关。下列说法正确的是( )
A.蛟龙号潜艇中携带过氧化钠的目的是杀菌消毒,保障呼吸安全卫生
B.市售“锌强化酱油”中含有大量锌元素
C.向燃煤中加入CaO、推广油电混合汽车、电动汽车均符合绿色化学理念
D.金属冶炼、金属单质的生成都是吸热反应,金属腐蚀、金属单质的消耗都是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com