
催化剂 | KClO3/g | 催化剂/g | 反应结束时间/s | 反应现象 |
MnO2 | 0.5 | 0.1 | 47 | 红热现象 |
Fe2O3 | 0.5 | 0.1 | 57 | 稳定 |
Cr2O3 | 0.5 | 0.1 | 67 | 由绿变黄 |
Al2O3 | 0.5 | 0.1 | 84 | 较慢 |
SiO2 | 0.5 | 0.1 | 181 | 缓慢 |
(注:红热现象指反应中有红色火光,反应剧烈并在短时间内结束)
(1)请你为这个实验拟定实验目的。
(2)你认为催化效果最好的是哪种,催化效果不好的是哪种?
(3)若要研究“催化剂的用量对催化效果的影响(用产生氧气的体积表示)”,请你设计实验的记录数据。
(1)实验目的是探究不同催化剂对催化效果的影响
(2)催化效果最好的是MnO2,催化效果不好的是SiO2。
(3)
催化剂 | KClO3/g | 反应时间/s | 催化剂/g | O2/V |
MnO2 | 0.5 | 47 |
|
|
MnO2 | 0.5 | 47 |
|
|
MnO2 | 0.5 | 47 |
|
|
解析:表中的数据有特征:不变的量是“KClO3的质量和催化剂的用量”;变化的量是“反应结束时间”(长短不同)和“反应现象”(剧烈程度不同)。比较这些“变量和不变量”知:(1)实验目的是探究不同催化剂对催化效果的影响;(2)反应从开始到结束的时间越短,催化效果越好。故催化效果最好的是MnO2,催化效果不好的是SiO2。(3)要研究“催化剂的用量对催化效果的影响”,则记录数据中不变的量是“KClO3的质量(如为0.5 g)和某催化剂(如MnO2)”,变化的量则是“催化剂的用量和产生氧气的体积”,实验的记录表格如下:
催化剂 | KClO3/g | 反应时间/s | 催化剂/g | O2/V |
MnO2 | 0.5 | 47 |
|
|
MnO2 | 0.5 | 47 |
|
|
MnO2 | 0.5 | 47 |
|
|


科目:高中化学 来源: 题型:阅读理解
| ||
| 微热 |

| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
查看答案和解析>>
科目:高中化学 来源:2012届甘肃省天水市二中高三模拟(5月)考试化学试卷(带解析) 题型:实验题
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
| 途径 | 生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| 1.Al→Al3+→Al(OH)3 | | |
2.Al→AlO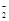 →Al(OH)3 →Al(OH)3 | | |
3.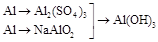 | | |
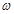 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入(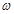 + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。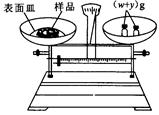
 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。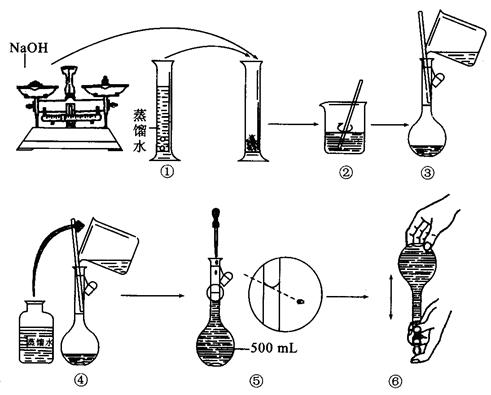
 NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。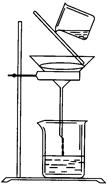
查看答案和解析>>
科目:高中化学 来源:2011-2012学年甘肃省天水市高三模拟(5月)考试化学试卷(解析版) 题型:实验题
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
|
途径 |
生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol |
|
|
消耗H+ |
消耗OH- |
|
|
1.Al→Al3+→Al(OH)3 |
|
|
|
2.Al→AlO |
|
|
|
3. |
|
|
(1)填写上表中空格并从节约原料的角度来分析,你认为应选择方案_________最为合理。
(2)本实验要用到NaOH溶液。某学生用已知质量y(g)的表面皿,准确称取 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入( + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。

(3)若称取的 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。

(4)阅读下列制备Al(OH)3实验步骤,填写空白:
①在烧杯A中加入50mL0.5mol·L NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
②在盛有适量稀H2SO4的烧杯B中应放入___________(g)(用含m1的式子表示)质量的铝屑,充分搅拌使铝屑反应完全。
③在盛有适量浓NaOH溶液的烧杯C中放入____________(g)(用含m1的式子表示)质量的铝屑充分搅拌使铝屑反应完全。
④将烧杯B和烧杯C中的溶液混和观察到的现象是:_______________________________,反应的离子方程式是:___________________________
(5)过滤时某学生操作如图,请用文字说明图中错误的是:
_____________________ 。

(6)把沉淀转移到烧杯中,用蒸馏水洗涤三次再过滤,再洗涤、
干燥得Al(OH)3固体质量为m2(g)计算本实验Al(OH)3的产率是_________________
查看答案和解析>>
科目:高中化学 来源:2010-2011学年云南省高三第二次毕业生复习统一检测(理综)化学部分 题型:实验题
硬质玻璃管是化学实验中经常使用的一种仪器,分析下列实验(固定装置及尾气处理过程均略去)并回答:
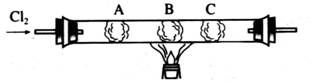
(1)如图所示,通入C12—段时间后,观察A、B、C三个棉球的变化,并补充完成下表所示的实验报告。
|
实验内容 |
实验现象[来源:Zxxk.Com] |
解释或结论 |
|
|
棉 球 |
棉球上滴加试剂 |
||
|
A |
KBr溶液 |
棉球变为___________色 |
化学方程式:__________ |
|
B |
_____溶液 |
棉球变为棕黄色 |
离子方程式:__________ |
|
C |
淀粉溶液 |
①棉球变为蓝色; ②待试管冷却后,在B、C之间的玻璃壁上有_____ 色固体产生 |
②的原因:__________ |
(2)实验室里,氯气通常用浓盐酸和二氧化锰在加热的条件下制取,该反应的化学方程
式为______________________________,此外还可以用高锰酸钾、氯酸钾等氧化剂与浓盐酸在常温下反应制取。某化学课外活动小组用如图所示的装置制取氯气并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸)。
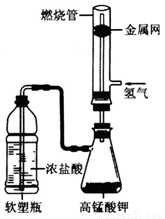
实验过程如下:
步骤一:先通入氢气,验纯后点燃;
步骤二:待氢气稳定燃烧后,挤压软塑瓶,将浓盐酸加入锥形瓶中,氢气持续安静燃烧。
请回答:
①步骤二完成后,火焰的颜色由淡蓝色变为__________色,燃烧管的上方可观察到_____现象;
②先通氢气并点燃,再通氯气的原因是_______________
③采用外管通氢气、内管通氯气的目的是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com