
【题目】一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是

A. 不能与FeCl3溶液发生显色反应
B. 1 mol该有机物最多可与3 mol H2加成
C. 1 mol该有机物最多可与含5 mol NaOH溶液反应
D. 1 mol该有机物与足量NaHCO3溶液反应可放出3 mol CO2
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵(NH4)2Fe(SO4)26H2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:(已知:FeS2与H2SO4不反应)

(1)莫尔盐属于____________。
A、酸式盐 B、碱式盐 C、复盐 D、硫酸盐
(2)硫铁矿焙烧的主反应是:4FeS2+11O2![]() 2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有__________,若150kg硫铁矿(FeS2质量分数为80%)完全反应转移电子数为________________________
2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有__________,若150kg硫铁矿(FeS2质量分数为80%)完全反应转移电子数为________________________
(3)加H2SO4酸浸,发生反应的离子方程式为________________________________。
(4)“还原”时,Fe3+可通过反应Ⅰ、Ⅱ被FeS2还原。
反应Ⅰ的离子方程式为:FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42—+16H+
反应Ⅱ的离子方程式为:_________________________________。
(5)为证明所得莫尔盐晶体中含有Fe2+和NH4+,实验方法是取其少量溶液于一支试管中,_______________证明含有Fe2+和NH4+。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为![]() ,下列关于该物质的说法中正确的是
,下列关于该物质的说法中正确的是
A. 该物质在NaOH的醇溶液中加热可转化为醇类
B. 该物质能和AgNO3溶液反应产生AgBr沉淀
C. 该物质可与溴的四氯化碳溶液发生加成反应
D. 该物质可以发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是_______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
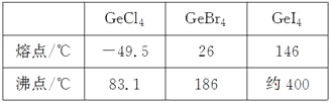
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为____________,微粒之间存在的作用力是________________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为________。
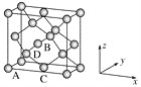
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。

提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新制氯水与久置的氯水相比较,下列结论不正确的是
A. 颜色相同B. 前者能使有色布条褪色
C. 都含有H+D. 加AgNO3溶液都能生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,下列说法正确的是( )
A. 氧化产物与还原产物物质的量之比是2∶5
B. 被氧化的HCl占参加反应HCl总分子数的![]()
C. KMnO4只有一部分发生还原反应
D. KMnO4与HCl恰好分别完全发生还原反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是( )
A.利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
B.只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液
C.用润湿的pH试纸测量某溶液的pH
D.实验室用NaOH溶液除去CO2中的少量HCl气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com