
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取不同质量样品溶于水后分别逐滴加入相同浓度盐酸30 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积)与加入样品的质量关系如图所示(不考虑CO2在水中的溶解、反应)。请计算:

(1)样品中n(Na2CO3) : n(NaHCO3)=____________。
(2)盐酸的物质的量浓度c(HCl)=________mol·L1。
【答案】2:1 2.5
【解析】
(1)根据图像,样品质量为2.96g时,生成气体为672mL(标准状况),Na2CO3和NaHCO3的完全反应,设2.96g混合物中Na2CO3、NaHCO3的物质的量分别为x、y,则①106g/mol×x+84 g/mol×y=2.96g、②x+y=![]() =0.03mol,联立①②解得:x=0.02mol、y=0.01mol,所以样品中物质的量之比n(Na2CO3)∶n(NaHCO3)=0.02mol∶0.01mol=2∶1,故答案为:2∶1;
=0.03mol,联立①②解得:x=0.02mol、y=0.01mol,所以样品中物质的量之比n(Na2CO3)∶n(NaHCO3)=0.02mol∶0.01mol=2∶1,故答案为:2∶1;
(2)根据图像,样品质量为6.66g生成气体为672mL,盐酸不足,碳酸钠优先反应生成碳酸氢钠,设6.66g样品中含有碳酸钠、碳酸氢钠的物质的量分别为2z、z,则106 g/mol×2z+84 g/mol×z=6.66g,解得:z=0.0225mol,即6.66g样品中含有0.045mol碳酸钠、0.0225mol碳酸氢钠,将样品加入盐酸中,先发生反应HCl+Na2CO3=NaHCO3+NaCl,0.045mol碳酸钠完全反应消耗HCl的物质的量为0.045mol,碳酸钠完全反应后再发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,生成标准状况下672mL二氧化碳消耗HCl的物质的量为:n(HCl)=n(CO2)=![]() =0.03mol,所以30mL盐酸中含有HCl的物质的量为:0.045mol+0.03mol=0.075mol,该盐酸的物质的量浓度为:c(HCl)=
=0.03mol,所以30mL盐酸中含有HCl的物质的量为:0.045mol+0.03mol=0.075mol,该盐酸的物质的量浓度为:c(HCl)= ![]() =2.5mol/L,故答案为:2.5。
=2.5mol/L,故答案为:2.5。


科目:高中化学 来源: 题型:
【题目】2014年德美科学家因开发超分辨荧光显微镜获诺贝尔化学奖,他们开创性的成就使光学显微镜分辨率步入了纳米时代。
Ⅰ.制纳米碳酸钙:在浓CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
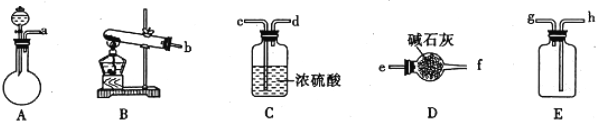
(1)实验室中若用浓氨水和生石灰制取并收集干燥的NH3,请选择装置并按气流方向连接各仪器接口___________(填装置接口顺序);若要制取并收集干燥的CO2,则需选用上述仪器装置中的_____________(填装置序号)。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是______,试写出制纳米级碳酸钙的离子方程式____________________________________。
Ⅱ.纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
(3)制备纳米TiO2:可将TiCl4水解产物经加热脱水制得纳米级TiO2。已知25℃时,Ksp[Ti(OH)4]=7.94×10-54,该温度下测得TiCl4溶液的pH=3,则此时溶液中c(Ti4+)=______________。
(4)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。配制NH4Fe(SO4)2标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的______________(填字母代号)。

(5)滴定終点的现象是______________________________________________________。
(6)滴定分析时,称取TiO2试样1.80g,消耗0.400mol·L-1 NH4Fe(SO4)2标准溶液45.00mL,则试样中TiO2的质量分数为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关钠及其化合物叙述错误的是。
A. 标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.1NA个
B. 1molNa2O2与足量的水反应,转移的电子数为2NA个
C. 常温下,2.3g钠投入到100mL水中,钠失去的电子数为0.1NA
D. 0.1mol钠在空气中完全燃烧生成Na2O2,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关分子结构 ![]() 的下列叙述中,正确的是
的下列叙述中,正确的是
A.可能在同一平面上的原子最多有20个
B.12个碳原子不可能都在同一平面上
C.所有的原子都在同一平面上
D.除苯环外的其余碳原子有可能都在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】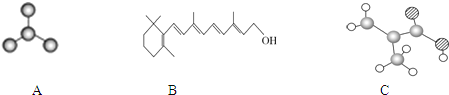
(1)图A是由4个碳原子结合成的某种烷烃(氢原子没有画出)。
①写出该有机物的系统命名法的名称_____________。
②该有机物的同分异构体的二氯取代物有_____________种。
(2)图B的键线式表示维生素A的分子结构。
①该分子的化学式为_____________。
②1mol维生素A最多可与_____________molH2发生加成反应。
(3)某物质只含C、H、O三种元素,其分子模型如图C所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
①该物质的结构简式为_____________。
②该物质中所含官能团的名称为_________________和_________________。
(4)下列实验操作不正确的是_________________
A.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液。
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验。
C.醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇
D.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制取乙酸乙酯
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动。
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种香料,存在于金橘中,可用如下路线合成:
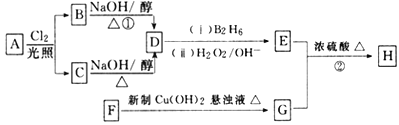
已知:R-CH=CH2![]() RCH2CH2OH (B2H6为乙硼烷)。
RCH2CH2OH (B2H6为乙硼烷)。
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以产生88gCO2和45gH2O。A的分子式是___________;
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为___________________;
(3)在催化剂存在下1molF与2molH2反应,生成3-苯基-1-丙醇。F的结构简式是__________________;
(4)反应①的反应类型是____________________;
(5)反应②的化学方程式为______________________________________________;
(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式_________________________________。(写任何一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将4molNH3和5molO2充入定容密闭容器中,在催化剂存在下进行下列反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=- 1025 kJ/mol,当达到平衡状态时,下列说法中正确的是
4NO(g)+6H2O(g) △H=- 1025 kJ/mol,当达到平衡状态时,下列说法中正确的是
A. 生成4molNO B. NH3和NO物质的量之和为4mol
C. 放出1025kJ的热量 D. 平衡时容器内气体压强和开始时压强相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com