

| A£® | µŚŅ»²½ŠčŃ”ÓĆŅĒĘ÷¢Ł”¢¢ŚŗĶ¢į£¬ŅĒĘ÷¢ŁµÄĆū³Ę½ŠŪįŪö | |
| B£® | µŚ¶ž²½ÓĆÅØĻõĖįČܽā²čŅ¶»Ņ£¬æÉÄܽ«Fe2+Ńõ»Æ³ÉFe3+ | |
| C£® | ŅŖĶź³ÉµŚČż²½£¬ŠčŃ”ÓĆ¢Ü”¢¢ŻŗĶ¢ß£¬³ż¼Š³ÖŅĒĘ÷Ķā»¹Č±ĀĖÖ½ | |
| D£® | µŚĖIJ½£¬ÓĆŹŌ¼Į¢ą¼ģŃéĀĖŅŗÖŠµÄFe3+£¬ČÜŅŗÖŠÉś³ÉŃŖŗģÉ«³Įµķ |
·ÖĪö ¼ģŃé²čŅ¶ÖŠµÄĢśŌŖĖŲ£¬ĻČ½«²čŅ¶ŌŚŪįŪöÖŠ×ĘÉÕ»Ņ»Æ£¬Č»ŗóŌŚÉÕ±ÖŠÓĆÅØĻõĖįČܽā²čŅ¶»Ņ²¢¼ÓÕōĮóĖ®Ļ”ŹĶ£¬ŌŚĀ©¶·ÖŠ¹żĀĖ£¬æÉȔɣĮæĀĖŅŗÓŚŠ”ŹŌ¹ÜÖŠ£¬ÓĆKSCNČÜŅŗ¼ģŃ飬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®½«²čŅ¶×ĘÉÕ»Ņ»Æ£¬Ó¦ŌŚŪįŪöÖŠ¼ÓČČ£¬ÓƵ½µÄŅĒĘ÷ÓŠ¢Ł”¢¢ŚŗĶ¢į£¬±ŲŅŖŹ±»¹æÉÓƵ½Čż½Å¼Ü»ņĢś¼ÜĢØ“ųĢśČ¦£¬ŅĒĘ÷¢ŁµÄĆū³Ę½ŠŪįŪö£¬¹ŹAÕżČ·£»
B£®ÅØĻõĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬Äܽ«Fe2+Ńõ»Æ³ÉFe3+£¬¹ŹBÕżČ·£»
C£®¹żĀĖŹ±ÓƵ½¢Ü”¢¢ŻŗĶ¢ß£¬¹ŹCÕżČ·£»
D£®µŚĖIJ½£¬ÓĆŹŌ¼Į¢ą¼ģŃéĀĖŅŗÖŠµÄFe3+£¬ČÜŅŗ±äĪŖŃŖŗģÉ«£¬Ć»ÓŠ³ĮµķÉś³É£¬¹ŹD“ķĪó£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģā²ąÖŲÓŚĪļÖŹµÄ¼ģŃéŗĶ¼ų±šµÄŹµŃéÉč¼ĘµÄ漲飬×ÅÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦£¬Āä½ÅÓŚ»ł“”ÖŖŹ¶µÄ漲飬עŅā°ŃĪÕŹµŃéµÄŌĄķ”¢²½ÖčŗĶŹµŃéŅĒĘ÷£¬ÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
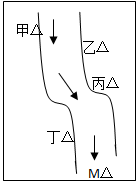 ŌŚŅ»ĢõÓćĻŗ¾ų¼£µÄŠ”ŗÓ±ßÓŠĖÄ׳¹¤³§£ŗ¼×”¢ŅŅ”¢±ū”¢¶”£ØČēĶ¼ĖłŹ¾£¬¼żĶ·±ķŹ¾ŗÓĖ®Į÷Ļņ£©£¬ĖüĆĒÅųöµÄ·ĻŅŗĄļ£¬Ćæøö¹¤³§Ö»ŗ¬ÓŠNa2CO3”¢FeCl3”¢Ca£ØOH£©2”¢HClÖŠµÄŅ»ÖÖ£®Ä³ÖŠŃ§»·±£Š”×é¶ŌŗÓĖ®¼ģ²āŹ±·¢ĻÖ£ŗ¢Ł¼×“¦ŗÓĖ®³ŹČé°×É«£¬¢ŚŅŅ“¦ŗÓĖ®³ŹŗģŗÖÉ«»ģ×Ē£¬¢Ū±ū“¦ŗÓĖ®ÓÉ»ė±äĒ壬¢Ü¶”“¦²śÉśĘųÅŻ£¬ŗÓĖ®ČŌĒ壬¢ŻM“¦Ė®ŃłµÄpHŠ”ÓŚ7£®
ŌŚŅ»ĢõÓćĻŗ¾ų¼£µÄŠ”ŗÓ±ßÓŠĖÄ׳¹¤³§£ŗ¼×”¢ŅŅ”¢±ū”¢¶”£ØČēĶ¼ĖłŹ¾£¬¼żĶ·±ķŹ¾ŗÓĖ®Į÷Ļņ£©£¬ĖüĆĒÅųöµÄ·ĻŅŗĄļ£¬Ćæøö¹¤³§Ö»ŗ¬ÓŠNa2CO3”¢FeCl3”¢Ca£ØOH£©2”¢HClÖŠµÄŅ»ÖÖ£®Ä³ÖŠŃ§»·±£Š”×é¶ŌŗÓĖ®¼ģ²āŹ±·¢ĻÖ£ŗ¢Ł¼×“¦ŗÓĖ®³ŹČé°×É«£¬¢ŚŅŅ“¦ŗÓĖ®³ŹŗģŗÖÉ«»ģ×Ē£¬¢Ū±ū“¦ŗÓĖ®ÓÉ»ė±äĒ壬¢Ü¶”“¦²śÉśĘųÅŻ£¬ŗÓĖ®ČŌĒ壬¢ŻM“¦Ė®ŃłµÄpHŠ”ÓŚ7£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠæŗĶŃĪĖįÉś³ÉĒāĘų | B£® | ĀČĖį¼ŲŗĶ¶žŃõ»ÆĆĢÉś³ÉŃõĘų | ||
| C£® | Ģ¼ĖįøĘŗĶŃĪĖįÉś³É¶žŃõ»ÆĢ¼ | D£® | ĀČ»ÆÄĘŗĶÅØĮņĖįÉś³ÉĀČ»ÆĒā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHCO3ŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½ĪŖNaHCO3=Na++H++CO32- | |
| B£® | NaHCO3ČÜŅŗÓėNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH++OH-=H2O | |
| C£® | NH4NO3ČÜŅŗÓėNaOHĻ”ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖNH4++OH-=NH3•H2O | |
| D£® | NH4NO3ČÜŅŗÓė×ćĮæBa£ØOH£©2ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖBa2++CO32-=BaCO3”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ļū»ÆĪĀ¶Č/”ę | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| ×Ŗ»ÆĀŹ/% | 50.3 | 58.2 | 85.1 | 85.2 | 90.7 | 91.2 | 91.5 |
| ĪļÖŹ | Mg£ØOH£©2 | Fe£ØOH£©3 | Fe£ØOH£©2 | Mn£ØOH£©2 |
| Ksp | 10-11 | 10-39 | 10-17 | 10-14 |

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com