
| A. | 碘水 | B. | 碘水、烧碱溶液、新制的Cu(OH)2 | ||
| C. | 氢氧化钠溶液、银氨溶液 | D. | 烧碱溶液、新制的Cu(OH)2 |
分析 淀粉在酶作用下水解生成葡萄糖,用新制的氢氧化铜悬浊液或银氨溶液可证明有无葡萄糖存在,根据淀粉水解的条件和产物验证的方法进行解答.
解答 解:淀粉在酶作用下水解生成葡萄糖,用新制的氢氧化铜悬浊液或银氨溶液可证明有无葡萄糖存在,证明淀粉在酶作用下只部分发生了水解的实验有两种方法:
一是:淀粉在稀硫酸作用下水解生成葡萄糖,加Na0H溶液中和稀硫酸,使混合液呈碱性,然后加入银氨溶液,有单质银生成可检验产物葡萄糖,证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全,故需实验试剂为碘水、烧碱溶液、银氨试剂;
二是:淀粉在稀硫酸作用下水解生成葡萄糖,加Na0H溶液中和稀硫酸,使混合液呈碱性,然后加入氢氧化铜悬浊液,最后再加热,有砖红色沉淀证明淀粉已水解,由水解后的溶液加碘水变蓝,则说明水解不完全,
故需实验试剂为碘水、烧碱溶液、氢氧化铜悬浊液;
故选B.
点评 本题考查了淀粉在酶作用下的水解,解答关键是检验淀粉和水解产物葡萄糖,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
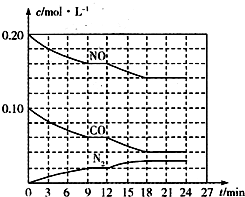 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.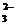 )+c(HSO
)+c(HSO )(用含硫微粒浓度的代数式表示).
)(用含硫微粒浓度的代数式表示).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
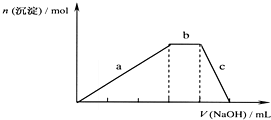
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2 H2O | |
| B. | CH4+2O2$\stackrel{点燃}{→}$CO2+H2O | |
| C. | 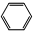 +HO-NO2$→_{△}^{浓硫酸}$ +HO-NO2$→_{△}^{浓硫酸}$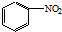 +H2O +H2O | |
| D. | CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2(g)+3H2(g)?2NH3(g) (正反应为放热反应) | |
| B. | C(s)+CO2(g)?2CO(g) (正反应为吸热反应) | |
| C. | 2NO2(g)?N2O4(g) (正反应为放热反应) | |
| D. | 3O2(g)?2O3(g) (正反应为吸热反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去NaCl固体中混有的MgCl2:加入KOH试剂后过滤 | |
| B. | 实验室获取少量纯净的水:蒸馏自来水 | |
| C. | 提纯混有少量硝酸钾的氯化钾:将混合物溶于热水中,再冷却、结晶并过滤 | |
| D. | 提取碘水中的碘:加入适量乙醇,振荡、静置、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
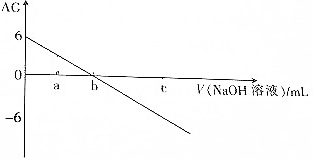
| A. | 若a点加入NaOH溶液的体积为10mL,则溶液中:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | b点加入NaOH溶液的体积为20mL | |
| C. | b点时,溶液中存在:c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| D. | 若c点加入NaOH溶液的体积为40mL,则溶液中:c(CH3COO-)+2c(CH3C00H)=c(OH-)-c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com