
| A. | 酒精 | B. | 蔗糖 | C. | 硝酸钾 | D. | 铜丝 |
科目:高中化学 来源:2016-2017学年河北省唐山市高二上10月月考化学试卷 (解析版) 题型:实验题
硫代硫酸钠(Na2S2O3)俗称大苏打,是一种重要的工业试剂。某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:(反应原理Na2S2O3+H2SO4===Na2SO4+H2O+SO2↑+S↓)
实验序号 | 反应温度(℃) | 参加反应的物质 | ||||
Na2S2O3 | H2SO4 | H2O | ||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(1)在上述实验中,反应速率最快的可能是______________(填实验序号)。
(2)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是__________(填实验序号,下同);
②A和B的组合比较,所研究的是__________因素对速率的影响,与该组合研究问题相同的组合是____________
③B和C的组合比较,所研究的问题是_________________。
(3)实验中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较(写出一个理由即可)____________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱溶液与小苏打溶液反应:OH-+HCO3-═H2O+CO2↑ | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氯气与水反应:H2O+Cl2═2H++Cl-+ClO- | |
| D. | 氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中可以得到NaCl电解熔融NaCl可制备金属钠 | |
| B. | 海水蒸发制海盐的过程中不涉及化学变化 | |
| C. | 从海水中提溴、碘、镁单质,都利用了氧化还原反应 | |
| D. | 利用潮汐发电是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室需用480mL、0.1mol/L的CuSO4溶液,应选用500mL容量瓶,称取12.5g胆矾 | |
| B. | 酸碱中和滴定实验中,锥形瓶用蒸馏水洗净后,需要用待测溶液润洗2-3次 | |
| C. | 溶解固体溶质或稀释溶液时,未冷却至室温即转入容量瓶进行定容 | |
| D. | 用标准浓度的NaOH 溶液滴定未知浓度的稀盐酸,碱式滴定管用蒸馏水润洗后不需要用标准溶液润洗2--3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器里P、Q、R、S四种物质共存 | |
| B. | 容器里气体总物质的量不再改变 | |
| C. | 容器内气体压强、密度不随时间变化 | |
| D. | 单位时间内生成nmol P同时生成nmol S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 糠醛(
糠醛(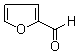 )可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O.
)可与新制含有NaOH的Cu(OH)2悬浊液在加热条件下反应得到砖红色沉淀Cu2O. 分子中含有σ键的数目为11mol.
分子中含有σ键的数目为11mol. 分子中碳原子轨道的杂化类型是sp2.
分子中碳原子轨道的杂化类型是sp2. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$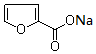 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com