
 某研究性学习小组根据老师的学案设计实验对碳酸钠和碳酸氢钠的性质进行研究.
某研究性学习小组根据老师的学案设计实验对碳酸钠和碳酸氢钠的性质进行研究.分析 (1)碳酸钠溶液与二氧化碳反应生成碳酸氢钠,据此书写离子方程式;
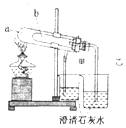
(2)碳酸氢钠稳定性差,加热易分解,而碳酸钠稳定性较强,加热时难以分解,加热大试管时,a处温度较高,最好在a试管底部加入碳酸钠;
(3)发生反应为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,利用差量法计算出混合物碳酸氢钠的质量,然后计算出碳酸钠的质量.
解答 解:(1)碳酸氢钠与二氧化碳发生反应生成碳酸氢钠,反应的离子方程式为:CO32-+H2O+CO2=2HCO3-,
故答案为:CO32-+H2O+CO2=2HCO3-;
(2)碳酸氢钠在小试管b,Na2CO3在大使管a,大试管直接加热,温度较高,如温度较高的不分解,而加热温度较低的物质分解,可判断稳定强弱,
故答案为:Na2CO3;
(3)设混合物中含有碳酸氢钠的质量为x,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑△m
168 62
x 27.4g-21.2g=6.2g
则:$\frac{168}{x}$=$\frac{62}{6.2g}$,
解得:x=16.8g,
原混合物中碳酸钠的质量为:27.4g-16.8g=10.6g,
答:原混合物中碳酸钠的质量是10.6g.
点评 本题考查物质检验与鉴别方案的设计,题目难度中等,明确碳酸钠、碳酸氢钠的性质为解答关键,注意掌握差量法的应用,试题培养了学生的分析能力及化学实验、化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑥⑦ | B. | ①②④⑤⑥ | C. | ⑤⑦ | D. | ④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
现有CO、CO2、O3(臭氧)三种气体,它们分别都含有1 mol氧原子,则三种气体的物质的量之比为( )
A.1:1:1 B.1:2:3 C.3:2:1 D.6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的物质的量浓度为1mol•L-1 | |
| B. | 配置该溶液需用MgCl29.5g | |
| C. | 该溶液与200mL1mol•L-1NaCl溶液的Cl-的物质的量浓度相同 | |
| D. | 取10mL该溶液再稀至100mL,所得溶液的Cl-的物质的量为0.02mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 16gCH4所含原子数目为5NA | |
| C. | 17gNH3所含电子数目为10NA | |
| D. | 在常温常压下,11.2LN2含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4 | B. | FeSO4•7H2O | C. | KAl(SO4)2•7H2O | D. | Fe2(SO4)3•7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. +Br2→
+Br2→ .
.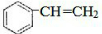 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$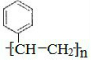 .
.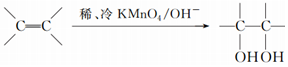 .请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式
.请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上教学质检化学试卷(解析版) 题型:实验题

(1)写出下列仪器的名称:①____________,②____________,④____________。
(2)仪器①~④中,使用时必须检查是否漏水的是________________(填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器____________,将仪器补充完整后进行的实验操作的名称为____________;②的进水口是____________(填“f”或“g”)。
(4)现需配制250mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com