
| A. | 将干冰放入冰箱 | B. | 让干冰在通风处自然升华 | ||
| C. | 直接将干冰倒入下水道 | D. | 用手取干冰扔入废物箱 |
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 6.4g由O3和O2组成的混合气体中一定含有0.4NA个原子 | |
| B. | 常温常压下,5.6g铁粉在7.1g氯气中充分燃烧,失去的电子数目为0.3NA | |
| C. | 常温下,pH=1的HNO3溶液中含有0.1NA个H+ | |
| D. | 0.1mol KHSO4晶体中含有的阳离子数是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{V}_{m}nb}{m{N}_{A}}$ | B. | $\frac{{V}_{m}mb}{n{N}_{A}}$ | C. | $\frac{{V}_{m}n{N}_{A}}{mb}$ | D. | $\frac{nb{N}_{A}}{{V}_{m}m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量少 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ | |
| D. | 在101 kPa时,H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2在101 kPa时的燃烧热为571.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 化合物 | A | B | C | D |
| Y | SiCl4 | Fe2O3 | H2O | FeCl3 |
| W | HCl | Al2O3 | NaOH | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含1molFeI2溶液中通入标准状况下22.4LCl22Fe2++2I-+2Cl2=2Fe3++I2+2Cl- | |
| B. | 在Na2S溶液中滴加少量FeCl3 2Fe3++S2-═2Fe2++S↓ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
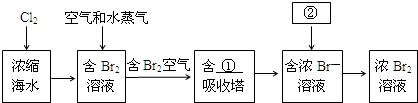
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com