
【题目】将钠投入到滴有无色酚酞溶液的水中,下列有关叙述中错误的是( )
A.Na浮在水面上
B.有气体产生
C.水溶液变为蓝色
D.Na熔化成小球并在水面上四处游动
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】“氢能”是未来最理想的新能源。
(1)实验测得,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则氢气燃烧热的热化学方程式为________(填选项字母)。
A.2H2(g)+O2(g)=2H2O(l) ΔH=-142.9 kJ·mol-1
B.H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
C.2H2O+O2=2H2O(l) ΔH=-571.6 kJ·mol-1
D.H2(g)+![]() O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
(2)某化学家根据“原子经济”的思想,设计了如下制备H2的反应步骤:
①CaBr2+H2O![]() CaO+2HBr
CaO+2HBr
②2HBr+Hg![]() HgBr2+H2
HgBr2+H2
③HgBr2+________![]() ________+________
________+________
④2HgO![]() 2Hg+O2↑
2Hg+O2↑
请你根据“原子经济”的思想完成上述步骤③的化学方程式:_____________;请根据“绿色化学”的思想评估该方法制H2的主要缺点:___________。
(3)利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。

请写出化学方程式:
反应①__________________________。
反应②__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10,现向1 L 0.2 mol·L-1HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中,正确的是
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. Ksp(CaF2)随温度和浓度的变化而变化
C. 该体系中没有沉淀产生
D. 该体系中HF与CaCl2反应产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入少量无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到乙试管中有明显现象时停止实验。试回答:

(1)试管乙中观察到的现象是______________________。
(2)液体混合加热时液体容积不能超过其容积_____,本实验反应开始时用小火加热的原因是__________;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(3)试管甲中加入浓硫酸的目的是__________。
(4)该实验中长导管的作用是_______,其不宜伸入试管乙的溶液中,原因是________。
(5)试管乙中饱和Na2CO3的作用是______________________________________。
(6)写出试管甲中发生反应的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列说法不正确的是( )

A. 反应前后各元素原子个数不变
B. 该反应说明分子在化学变化中可以再分
C. 该反应的生成物只有一氧化碳和氢气
D. 反应前后各元素化合价均不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】龙葵醛是一种珍贵的香料,广泛应用于香料、医药、染料及农药等行业。其合成路线如图所示(部分反应产物和反应条件已略去)。

回答下列问题:
(1)X的名称是_______
(2)下列有关龙葵醛和C3H6(烯烃)的说法正确的是________(填序号)。
A.它们的实验式相同 B.它们都能使溴水褪色
C.它们都能发生加成反应 D.它们都含有碳碳双键
(3)反应⑤的试剂和条件是________,反应③的反应类型是__________。
(4)有机物T所含官能团的名称是________,反应④的化学方程式为__________。
(5)在T的同分异构体中,遇氯化铁溶液发生显色反应的有_____种,其中,在核磁共振氢谱上有4 组峰且峰的面积之比为1:2 :3 :6 的结构简式为_________(写出其中的一种)。
(6) 参照上述流程图(如R![]() X……),以2-甲基-1,3-丁二烯为原料,经三步制备2-甲基-1,4-丁二醛,设计合成路线:________________。
X……),以2-甲基-1,3-丁二烯为原料,经三步制备2-甲基-1,4-丁二醛,设计合成路线:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+ Na+ |
阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:

(1)M为电源的__________极(填“正”或“负”)。
(2)写出甲烧杯中反应的化学方程式____________________。
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的_________(填“M”或“N”)极。

(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。该设想中负极的电极反应式为 __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生物电化学方法脱除水体中NH4+的原理如下图所示:
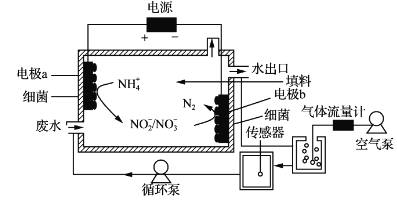
下列说法正确的是
A. 装置工作时,化学能转变为电能
B. 装置工作时,a极周围溶液pH降低
C. 装置内工作温度越高。NH4+脱除率一定越大
D. 电极b上发生的反应之一是:2NO3--2e-=N2↑+3O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。下列说法不正确的是

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及极性键的断裂与生成
C. 氧化剂与还原剂的物质的量之比为1∶3
D. 原料气N2可通过分离液态空气获得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com