
| 0.1g |
| 0.2g |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(14��)��ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuCl2��3H2O��CaCO3�IJ������£�
Ϊ����й����⣬��ȤС��ͬѧ����й����ʳ�����pH�������£�
| ���� | pH (��ʼ����) | pH(��ȫ����) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
�š����ӡ�ʱ��ͨ������Cl2��Fe2��������Fe3�����ټ���CuO���������Һ��pH�� (��д��Χ)������Fe(OH)3�Ƿ������ȫ��ʵ�鷽���� ��
�Ʋ���X���� �� �����˺�ϴ�ӵȡ�CuCl2��3H2O�������յ����ղ���Ļ�ѧʽ�� ��
��ij��θҩƬ�������ΪCaCO3����ҩƬ��CaCO3���������IJⶨ�������£�
a������0.1mol��L��1��HCl��Һ��0.1mol��L��1��NaOH��Һ��250mL��
b��ȡ0.1gĥ����θҩ����ƿ�С�
c������ƿ�ڼ���25.00mL 0.1 mol��L��1��HCl��Һ��
d���Է�̪Ϊָʾ������0.1mol��L��1��NaOH��Һ�ζ������ﵽ�ζ��յ㡣
e���ظ�bcd�����IJ���2�Ρ�
�� ����c����ȡ��������������� ��
�� ��ϴ�Ӻ�ļ�ʽ�ζ���δ��NaOH��Һ��ϴ��������CaCO3������������ (ѡ�ƫ����ƫС������Ӱ�족)��
�� ���ζ���NaOH��Һ��ƽ������Ϊ15.00mL����θҩ��̼��Ƶ���������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ�ϸԸ���ѧ�߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
(14��)��ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuCl2��3H2O��CaCO3�IJ������£�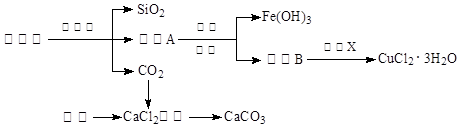
Ϊ����й����⣬��ȤС��ͬѧ����й����ʳ�����pH�������£�
| ���� | pH (��ʼ����) | pH(��ȫ����) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(14��)��ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuCl2��3H2O��CaCO3�IJ������£�

Ϊ����й����⣬��ȤС��ͬѧ����й����ʳ�����pH�������£�
|
���� |
pH (��ʼ����) |
pH(��ȫ����) |
|
Fe(OH)3 |
1.9 |
3.2 |
|
Fe(OH)2 |
7.0 |
9.0 |
|
Cu(OH)2 |
4.7 |
6.7 |
�š����ӡ�ʱ��ͨ������Cl2��Fe2��������Fe3�����ټ���CuO���������Һ��pH�� (��д��Χ)������Fe(OH)3�Ƿ������ȫ��ʵ�鷽���� ��
�Ʋ���X���� �� �����˺�ϴ�ӵȡ�CuCl2��3H2O�������յ����ղ���Ļ�ѧʽ�� ��
��ij��θҩƬ�������ΪCaCO3����ҩƬ��CaCO3���������IJⶨ�������£�
a������0.1mol��L��1��HCl��Һ��0.1mol��L��1��NaOH��Һ��250mL��
b��ȡ0.1gĥ����θҩ����ƿ�С�
c������ƿ�ڼ���25.00mL 0.1 mol��L��1��HCl��Һ��
d���Է�̪Ϊָʾ������0.1mol��L��1��NaOH��Һ�ζ������ﵽ�ζ��յ㡣
e���ظ�bcd�����IJ���2�Ρ�
�� ����c����ȡ��������������� ��
�� ��ϴ�Ӻ�ļ�ʽ�ζ���δ��NaOH��Һ��ϴ��������CaCO3������������ (ѡ�ƫ����ƫС������Ӱ�족)��
�� ���ζ���NaOH��Һ��ƽ������Ϊ15.00mL����θҩ��̼��Ƶ���������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�����и߶����ϣ���ĩ��ѧ�Ծ��������棩 ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com