
| A. | Cu是原电池的负极 | |
| B. | 电流由Cu电极流出 | |
| C. | 电子由Al沿导线流向Cu | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
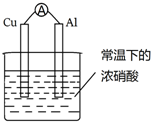
分析 铜、铝、浓硝酸构成的原电池中,金属铝遇到浓硝酸会发生钝化,所以金属铜是负极,金属铝是正极,负极上金属失电子发生氧化反应,正极上是得电子的还原反应.
解答 解:A、铜、铝、浓硝酸构成的原电池中,金属铝遇到浓硝酸会发生钝化,所以金属铜是负极,金属铝是正极,故A正确;
B、以金属铜是负极,金属铝是正极,所以电流由正极铝流出,故B错误;
C、电子从负极流向正极,即从铜流向铝,故C错误;
D、铝是正极,该电极上金属不会反应,是硝酸中的硝酸根离子发生得电子的还原反应,故D错误.
故选A.
点评 本题考查学生原电池的构成条件以及工作原理的应用知识,注意金属铝常温下遇到浓硝酸会发生钝化的知识是关键,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡是一个动态平衡 | |
| B. | 化学平衡研究的对象主要是可逆反应 | |
| C. | 化学反应速率是研究化学反应进行的快慢问题,化学平衡是研究化学反应进行的限度问题 | |
| D. | 化学反应达到平衡时,正反应和逆反应速率相等,是对反应中不同物质而言 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇在电池的负极上参加反应 | |
| B. | 1 mol C2H5OH被氧化时,有6 mol电子转移 | |
| C. | 随着反应的进行,正极附近溶液的酸性减弱 | |
| D. | 电池的正极反应为2H2O+O2+4e- 4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol (反应热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=+116.2kJ/mol (反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SO2+2H2S═3S↓+2H2O | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型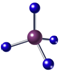 | |
| B. | Cl-的结构示意图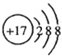 | |
| C. | 中子数为8的碳原子的核素符号为12C | |
| D. | 中子数为1的氢原子的核素符号为21H |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com