

���� ��1������������μӻ������ʵ�飬ʵ��ǰһ��Ҫ���װ�õ������ԣ��Է�װ��©��Ӱ��ʵ������װ�������Լ���ԭ��һ����ͨ��ѹǿ�����������Ե��������жϣ�
��2����A���Ƶõ��������������Ȼ��⡢ˮ����������ͨ��ʢ�б���ʳ��ˮ����Ũ�����ϴ��ƿ��ȥ��
��3��װ�ã�A���з�����Ӧ�Ļ�ѧ����ʽ�Ƕ������̺�Ũ���ᡢ�Ȼ��ƹ�����ȷ�Ӧ���������������ж������������ƽ���β���������չ�����������
��� �⣺��1��װ�������Լ��ķ�����װ�����Ӻú�����ĩ�˷���ʢˮ���ձ��У��þƾ�������ƿ���ձ��еĵ��ܿ�������ð����ֹͣ���ȣ����ܿڲ��γ�һ��ˮ������������װ�ò�©����
�ʴ�Ϊ���رշ�Һ©��������װ�����Ӻú�����ĩ�˷���ʢˮ���ձ��У��þƾ�������ƿ���ձ��еĵ��ܿ�������ð����ֹͣ���ȣ����ܿڲ��γ�һ��ˮ������������װ�ò�©����
��2����A���Ƶõ��������������Ȼ��⡢ˮ����������ͨ��ʢ�б���ʳ��ˮ����Ũ�����ϴ��ƿ��ȥ��װ��E������������Һ��ʣ�������ͨ������������Һ ���ն�����������ֹ��Ⱦ������
�ʴ�Ϊ������ʳ��ˮ����ȥCl2�е�HCl��Ũ�����ȥCl2�е�ˮ����������������Һ ���ն�����������ֹ��Ⱦ��
��3��װ�ã�A���з�����Ӧ�Ļ�ѧ����ʽ�Ƕ������̺�Ũ���ᡢ�Ȼ��ƹ�����ȷ�Ӧ������������Ӧ�Ļ�ѧ����ʽΪ��2NaCl+3H2SO4��Ũ��+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$2NaHSO4+Cl2��+MnSO4+H2O��װ��E���������������Ʒ�Ӧ����ֹ��Ⱦ��������Ⱦ��������Ӧ�Ļ�ѧ����ʽΪ��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��2NaCl+3H2SO4��Ũ��+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$2NaHSO4+Cl2��+MnSO4+H2O��Cl2+2NaOH=NaCl+NaClO+H2O��
���� ������������ʵ���Һ����ʵļ������飬����ؼ���������������ʣ��ͳ��������Ʊ��������ơ�����ķ������Ǹ߿����ȵ㣬��Ŀ�Ѷ��еȣ�


 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������CaCl2��Һ�������˰�ɫ����������Һ��һ�����д�����CO32- | |
| B�� | NaCl��Һ��Na2CO3��������ʱ������ɫ��ͬ | |
| C�� | ͨ�����ȵ�CuO����ʹ�����ɺڱ�������һ����H2 | |
| D�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �� | �� | �� | �� | �� |
| ���� | ʳ�� | �� | ����ˮ | ʯ��ˮ | ������Һ |
| ��Ҫ�ɷ� | CH3COOH | C2H5OH | C12H22O11 | Ca��OH��2 | Na2CO3 |
| ��ҺPH | 3 | 7 | 7 | 11 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� �Լ� | T1/�� | T2/�� | T2/�� |
| Ha2CO2 | 23.3 | 20.0 | 23.7 |
| HaCO2 | 18.5 | 20.0 | 20.8 |
| �¶� �ܽ�� | 10�� | 20�� | 30�� | 40�� |
| Ha2CO2 | 12.5g | 21.5g | 39.7g | 40��g |
| HaHCO2 | 8.1g | 9.6g | 11.1g | 12.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �� | �� | �� | �� | �� | �� |
| ������װ��ͼ | 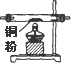 |  |  |  | 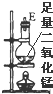 |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�2.54 g����ʱ������NaOH��Һ�������600 mL | |
| B�� | ��Ũ������HNO3�����ʵ���Ũ����14.0 mol/L | |
| C�� | NO2��N2O4 �Ļ�������У�NO2�����������80% | |
| D�� | �úϽ���ͭ��þ�����ʵ���֮����2��1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com