
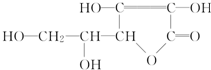
 维生素C的结构简式如图所示:
维生素C的结构简式如图所示: 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
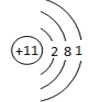 ,G在元素周期表中的位置为第三周期第ⅤⅡA族.
,G在元素周期表中的位置为第三周期第ⅤⅡA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 用途 | 解释 |
| A | 晶体硅 | 高纯硅广泛用于光导纤维、太阳能电池和计算机芯片 | 硅具有半导体性能 |
| B | 氧化铝 | 制作耐高温材料 | Al2O3熔点很高 |
| C | 硫酸钡 | 医学上用做钡餐 | Ba无毒 |
| D | 明矾 | 作消毒剂 | 明矾水解产生具有吸附性的胶体粒子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24 L H2O中含有极性共价键的数目为0.2 NA | |
| B. | 0.1 mol•L-1 NH4Cl溶液中含有NH4+的数目小于0.1 NA | |
| C. | 100 mL 12 mol•L-1的浓HNO3与过量Cu反应转移电子的数目为0.6 NA | |
| D. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可消除对大气的污染 | |
| B. | 可节约燃料 | |
| C. | 可缓解能源危机 | |
| D. | 此题中的CH4、CH3OH、NH3等为一级能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用活性炭去除冰箱中的异味 | |
| B. | 用热碱水清除炊具上残留的油污 | |
| C. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| D. | 用含硅胶、铁粉的透气小袋与食品一起密封包装 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
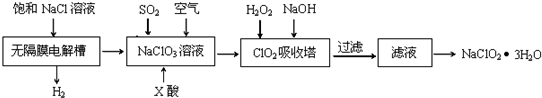

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com